��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��1��105Pa��298 K�����£�2mol����ȼ������ˮ�����ų�484 kJ�����������Ȼ�ѧ����ʽ��ȷ����
[? ]
A��H2O��g����H2��g����1/2O2��g����H �� ��242kJ/mol
B��2H2��g����O2��g����2H2O��l����H �� ��484kJ/mol
C��H2��g����1/2O2��g����H2O ��l����H �� ��242 kJ/mol
D��2H2��g����O2��g����2H2O��g����H �� ��484 kJ/mol
�ο��𰸣�A
���������
�����Ѷȣ���
2������� (15��)������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
(1)1molN2(��̬)������H2 (��̬)��Ӧ������ NH3(��̬)���ų�92.2 kJ��������
(2)���Ƿ���ʱ����N2H4Ϊȼ�ϡ�1molN2H4(��̬)��O2 (��̬)��ȼ�գ�����N2 (��̬)��H2O(��̬)���ų�534kJ��������
(3).��101kPaʱ��4.0g�����O2����ȫȼ������SO2���ų�37kJ������,S��ȼ����Ϊ______��Sȼ�յ��Ȼ�ѧ����ʽΪ_____ _��
�ο��𰸣�(��15��)
(1)N2(g) +3H2(g) ="=" 2NH3(g)����H =" -99.2" kJ/mol
(2)N2H4(g) + O2(g) ="=" N2(g) + 2H2O(g)����H = -534kJ/mol
(3)296 kJ/mol S(s) + O2(g) SO2����H =" -296" kJ/mol
SO2����H =" -296" kJ/mol
��������������Ȼ�ѧ����ʽ����д����Ӧ�ȵ��йؼ���ȡ��Ȼ�ѧ����ʽ�DZ�ʾ��ѧ��Ӧ�뷴Ӧ�ȹ�ϵ�ķ���ʽ����д��Ӧ���Ȼ�ѧ����ʽʱ����ע�����¼��㣺
��������ȷд����Ӧ�ļ�������ʽ�������ʻ�ѧʽǰ�Ļ�ѧ����ϵ��������������Ҳ�����Ƿ�����
�����ڸ����ʻ�ѧʽ�Ҳ���Բ���������������ʵľۼ�״̬��������g��l��s�ֱ������̬��Һ̬����̬�������в�ͬ��̬ʱ�����轫��̬ע��������S��б������S����б����C��ʯī����C�����ʯ���ȡ���Һ�еķ�Ӧ���ʣ�����ע����Ũ�ȣ���aq����ˮ��Һ��(aq) ��������ϡ��ˮ��Һ��
�����۷�Ӧ���뷴Ӧ����ʽ���Ӧ������Ӧʽ����д��ʽ��ͬ������Ӧ�Ļ�ѧ����ϵ����ͬ���ʷ�Ӧ���ͬ����
���Ȼ�ѧ����ʽ���������Ӧ��Ũ�ȡ��¶Ⱥ�ѹ�������������ڳ��³�ѹʱ��ʡ�ԡ�
��1��1molN2(��̬)������H2 (��̬)��Ӧ������ NH3(��̬)���ų�92.2 kJ�����������Ը÷�Ӧ���Ȼ�ѧ����ʽ��N2(g) +3H2(g) ="=" 2NH3(g) ��H =" -99.2" kJ/mol��
��2��1molN2H4(��̬)��O2 (��̬)��ȼ�գ�����N2 (��̬)��H2O(��̬)���ų�534kJ�����������Ը÷�Ӧ���Ȼ�ѧ����ʽ��N2H4(g) + O2(g) ="=" N2(g) + 2H2O(g) ��H = -534kJ/mol��
��3��ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų���������4.0g�����O2����ȫȼ������SO2���ų�37kJ����������1mol�����O2����ȫȼ������SO2���ų���������37kJ��32/4��296 kJ������S��ȼ������296 kJ/mol���÷�Ӧ���Ȼ�ѧ����ʽ��S(s) + O2(g) SO2 ��H =" -296" kJ/mol��
SO2 ��H =" -296" kJ/mol��
�����Ѷȣ�һ��
3��ѡ���� ����������Ӧ���Ȼ�ѧ����ʽ��
��I2��g��+H2��g��?2HI��g����H=-9.48kJ?mol-1
��I2��s��+H2��g��?2HI��g����H=+26.48kJ?mol-1
����˵����ȷ���ǣ�������
A���ٵIJ���ȢڵIJ����ȶ�
B��I2��s��=I2��g����H=+17.00kJ?mol-1
C���ڵķ�Ӧ���������Ȣٵķ�Ӧ����������
D��1molI2��g����ͨ��1molH2��g����������Ӧʱ����9.48kJ
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� 16. ���и����Ȼ�ѧ����ʽ�У���H1> ��H2 ����
��C(s)��O2(g)===CO2(g) ��H1 C(s)��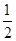 O2(g)===CO(g) ��H2
O2(g)===CO(g) ��H2
��S(s)��O2(g)===SO2(g) ��H1 S(g)��O2(g)===SO2(g) ��H2
��H2(g)��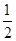 O2(g)===H2O(l) ��H1 2H2(g)��O2(g)===2H2O(l) ��H2
O2(g)===H2O(l) ��H1 2H2(g)��O2(g)===2H2O(l) ��H2
��CaCO3(s)===CaO(s)��CO2(g) ��H1 CaO(s)��H2O(l)===Ca(OH)2(s) ��H2
A����
B����
C���ڢۢ�
D���٢ڢ�