微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 16O与18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是
A.16O与18O互为同分异构体
B.16O与18O核外电子排布方式不同
C.通过化学变化可以实现16O与18O间的相互转化
D.标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子
参考答案:D
本题解析:
正确答案:D
A、不正确,16O与18O是氧的两种核素,互为同位素;
B.不正确,16O与18O核外电子数相同,核外电子排布方式相同,均为1s22s22p4
C.不正确,通过化学变化无法实现16O与18O间的相互转化,只有通过核反应才能实现;
D.正确。
本题难度:一般
2、选择题 下列物质中标*号的原子为sp3杂化的是( )
A.H2O
B.H3
C.F3
D.
参考答案:B
本题解析:ACD均是平面型结构,属于sp2杂化。氨气中氮原子有1对孤对电子,是sp3杂化。答案选B。
本题难度:一般
3、选择题 根据下表部分短周期元素的信息,判断相关叙述正确的是
元素代号?
| L
| M
| Q
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.089
| 0.102
| 0.074
|
主要化合价
| +2
| +3
| +2
| +6、-2
| -2
|
?
A.氢化物的稳定性:H2T<H2R
B.L的金属性比Q强
C.L与T形成的化合物属于离子化合物
D.L和M两者最高价氧化物对应的水化物能相互反应
参考答案:BC
本题解析:由于最低负价=主族序数―8,电子层数越多半径越大,则T、R分别是第VIA族的氧、硫,氧的非金属性比硫强,则气态氢化物的稳定性:H2O>H2S,故A错误;最高正价=主族序数,则L、Q分别是第IIA族的镁、铍,镁的金属性比铍强,故B正确;Mg是活泼金属,O是活泼非金属,二者形成的MgO是离子化合物,故C正确;M位于第IIIA族,原子半径比镁小,比铍大,说明它是铝,镁、铝的最高价氧化物对应的水化物分别是氢氧化镁,氢氧化铝,前者属于中强碱,后者属于两性氢氧化物,因此二者不能反应,故D错误。
本题难度:一般
4、选择题 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是(?)

A.X的气态氢化物比Y的稳定
B.W的最高价氧化物对应水化物的酸性比Z的强
C.Z的非金属性比Y的强
D.X与Y形成的化合物都易溶于水
参考答案:B
本题解析:由题意知Y为氧元素O,则X、Y、Z、W分别为:N、O、S、Cl。N与O元素形成的NO不可溶于水。
本题难度:一般
5、填空题 16分)现有六种短周期元素A、B、C、D、E、F,其原子序数依次增大,其中B与C、D与F分别位于同一周期,A与D、C与F分别位于同一主族,且A、D两元素原子的质子数之和是C、F两元素原子质子数之和的一半。又知六种元素所形成的常见单质在常温常压下三种是气体,三种是固体。请回答下列问题:
(1)D离子的结构示意图?;
F元素氧化物的晶体类型为?。
(2)比较B、C、D元素简单离子半径的大小:?>?>?(填微粒符号)
(3)请说出C的氢化物比F的氢化物稳定的根本原因:?;
用高能射线照射液态水时,一个A2C分子能释放出一个电子,同时产生一种具有较
强的氧化性的阳离子,试写出阳离子的电子式:?,该阳离
子中存在的化学键有?,并写出该阳离子与F氢化物的水溶
液反应的离子方程式:?。
(4)E是金属元素,且E单质可以与空气中的N2、CO2等反应 ,E的最高价氧化物的水化物难溶于水,已知298K时,该难溶物质的的KSP=5.6×10-12,若此时测得溶液pH
,E的最高价氧化物的水化物难溶于水,已知298K时,该难溶物质的的KSP=5.6×10-12,若此时测得溶液pH
=13.00,则此温度下残留在溶液中的E离子物质的量浓度为?mol・L-1。?
参考答案:
(1)D离子的结构示意图 ? F元素氧化物的晶体类型为分子晶体
? F元素氧化物的晶体类型为分子晶体
(2)N3->O2->Na+
(3)O的非金属性比S强
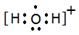 ,化学键有共价键?2H2O+ + H2S =" S" + 2H2O?+ 2H+
,化学键有共价键?2H2O+ + H2S =" S" + 2H2O?+ 2H+
(4)5.6*10-10mol・L-1。
本题解析:略
本题难度:一般