微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于电负性的叙述中不正确的是( )
A.电负性用来描述不同元素的原子对键合电子吸引力的大小
B.电负性是以氟为4.0、锂为1.0作为标准的相对值
C.元素电负性越小,元素金属性越强
D.元素电负性越大,元素非金属性越强
参考答案:C
本题解析:钙的金属性强于钠的,但电负性也大于钠的,所以选项C不正确,其余选项都是正确的,答案选C。
点评:该题是基础性试题的考查,试题难易适中,注重基础,侧重能力的培养和训练。该题的关键是明确电负性的含义和变化规律,然后灵活运用即可。
本题难度:一般
2、选择题 下列物质的熔点高低顺序,正确的是
A.金刚石>晶体硅>碳化硅
B.K>Na
C.HCHO<CH3OH
D.KF<KCl<KBr
参考答案:C
本题解析:A中形成的晶体都是原子晶体。由于键长C-C<C-Si<Si-Si,则熔点为金刚石>碳化硅>晶体硅,故A错误; B中形成的晶体都是金属晶体,由于K、Na的电荷相同,钠原子半径<钾原子半径,则熔点为Na>K,股B错误;C中形成的都是分子晶体,甲醇分子间存在氢键,则甲醇的熔点高于甲醛的,C正确;D中形成的都是离子晶体,由于离子半径F-<C-<Br-,则熔点为KF>KCl>KBr,故D错误,答案选C。
点评:该题是中等难度的试题,也是高考中的常见考点,试题针对性强,注重基础,有利于培养学生的逻辑推理能力,提高学生的学习效率。明确不同类型晶体熔点的比较方法是解答本题的关键。
本题难度:一般
3、选择题 能够一次性操作就能鉴别Na2SO3、BaCl2、NaCl、Na2CO3四种物质的一种试剂是
A.AgNO3
B.稀H2SO4
C.稀HCl
D.稀HNO3
参考答案:B
本题解析:试题分析:硝酸银和四种都反应生成白色沉淀,不能鉴别;稀硫酸和亚硫酸钠反应生成无色由刺激性气味的SO2,和氯化钡反应生成白色沉淀硫酸钡,和氯化钠不反应,和碳酸钠反应生成无色无味的CO2,可以鉴别;稀盐酸只能鉴别碳酸钠和亚硫酸钠;同样稀硝酸只能鉴别碳酸钠和亚硫酸钠,所以答案选B。
考点:考查物质的的鉴别
点评:该题是中等难度的试题,试题贴近高考,注重能力的考查和培养。该题的关键是明确进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
4、填空题 已知A、B、C、D分别是由短周期元素组成的四种微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒。请回答下列问题:
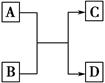
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:_________________________________________________________________。
(2)若B、D属于同主族元素形成的单质分子,写出C的化学式:________。
(3)若A、B均是含有2个原子核的微粒,且B中含有10个电子,D中含有18个电子,则A、B之间发生反应的离子方程式为___________________________________________________。
(4)若D是一种含有22电子的分子,则符合如图所示转化关系的A为________________(写出物质的化学式,如果是有机物则写出相应的结构简式)。
参考答案:(1)2F2+2H2O=4HF+O2 (2)H2O (3)HS-+OH-=S2-+H2O (4)CH3CH3(或CH3OH)
本题解析:(1)因A是一种含有18电子的微粒,C是一种含有10电子的微粒,且A与B之间发生了置换反应,所以A为F2,B为H2O,C为HF,D为O2。(2)因B、D属于同主族元素形成的单质分子,且A是一种含有18电子的微粒,C是一种含有10电子的微粒,故该条件下A为H2S,B为O2,C为H2O,D为S。(3)因A、B均是含有2个原子核的微粒,且B中含有10个电子,D中含有18个电子,故A为HS-,B为OH-,C为H2O,D为S2-。(4)因D是一种含有22电子的分子,常见的含22电子的分子主要是CO2和N2O;结合题给的信息分析,本题中的D只能为CO2,故对应的A可能为乙烷或甲醇。
本题难度:一般
5、选择题 短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数的差是8,A原子的最外层电子数是其次外层电子数的3倍,在同周期主族元素中B原子的原子半径最大。下列说法正确的是
A.气态氢化物的热稳定性:A<C
B.元素A与B只能形成一种化合物
C.元素B与D形成的化合物是离子化合物
D.最高价氧化物对应的水化物的酸性:C>D
参考答案:C
本题解析:A、B、C、D分别为O、Na、S、Cl。A、非金属性S<O,故H2O稳定性强于H2S ,错误;B、可以形成氧化钠和过氧化钠,错误;C、正确;D、非金属性S<Cl,H2SO4酸性弱于HClO4,错误。
本题难度:一般