微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 碘在科研与生活中有重要应用。某兴趣小组用0.50mol・L-1KI、0.2%淀粉溶液、0.20mol・L-1K2S2O8、0.10mol・L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I-
参考答案:
本题解析:
本题难度:一般
2、选择题 下列肯定能使化学反应速率增大的措施是
[? ]
A.增加反应物的量
B.增大压强
C.升高温度
D.使用催化剂
参考答案:C
本题解析:
本题难度:一般
3、填空题 Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快.由此判断,影响化学反应速率的因素有______和______.
参考答案: 因当加热或加入浓盐酸后,反应速率明显加快,所以影响化学反应速率的因素有温度和浓度.故答案为:温度;浓度.
本题解析:
本题难度:一般
4、实验题 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。
序号
| 条件
| 现象
| 结论
|
温度/℃
| 催化剂
|
1
| 40
| FeCl3溶液
|
|
|
2
| 20
| FeCl3溶液
|
|
|
3
| 20
| MnO2
|
|
|
4
| 20
| 无
|
|
|
试回答:实验1、2研究的是其他条件相同时 对H2O2分解速率的影响。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________。

②定量分析:为了更精确地研究浓度对反应速率的影响,利用乙图装置进行定量实验。完成该实验应该测定的实验数据是____________________________________________。
参考答案:(1)(1)温度
(2) ①反应产生气泡的快慢 控制阴离子相同,排除阴离子的干扰
② 测定一定时间内产生的气体(测定产生一定体积气体所需要的时间)
本题解析:
(1)由表格信息可知研究对象是温度。
(2)①定性分析时,只需要观察反应产生气泡的快慢,改用Fe2(SO4)3,避免阴离子的干扰。
②测定一定时间内产生的气体(测定产生一定体积气体所需要的时间)
考点:考查了实验的基本操作原理和实验的分析。
本题难度:困难
5、实验题 H2O2是实验室常用的一种化学试剂。某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号
| 反应物
| 催化剂
|
①
| 10mL2% H2O2溶液
| 无
|
②
| 10mL5% H2O2溶液
| 无
|
③
| 10mL5% H2O2溶液
| 1mL0.1mol・L-1FeCl3溶液
|
④
| 10mL5% H2O2溶液+少量HCl溶液
| 1mL0.1mol・L-1FeCl3溶液
|
⑤
| 10mL5% H2O2溶液+少量NaOH溶液
| 1mL0.1mol・L-1FeCl3溶液
|
(1)实验①和②的目的是_? ? ,
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。分析下图能够得出的结论是?。
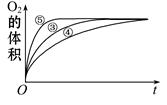
(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如下图所示的实验装置进行实验。
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是?。

(4)H2O2能氧化H2SO4?酸化的FeSO4,离子方程式为?;
参考答案:(8分)(1)探究H2O2溶液的浓度的变化对分解速率的影响。
(2)图像显示FeCl3溶液的催化作用,碱性条件下效果较好,酸性条件下效果较弱。
(3)测量出分别在Fe3+和Cu2+的催化作用下,收集40mL气体的始、终时间,就能计算出反应速率。
(4)Fe2++2H2O2+4H+= Fe3++4H2O
本题解析:(1)根据表中数据可知,实验①②中不同之处在于双氧水的浓度不同,所以实验目的是探究H2O2溶液的浓度的变化对分解速率的影响。
(2)由图可知,⑤的反应速率最大,④的反应速率最小,结合实验方案可知,碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率,即实验结论是图像显示FeCl3溶液的催化作用,碱性条件下效果较好,酸性条件下效果较弱。
(3)要比较Fe3+和Cu2+对H2O2分解的催化效果,应在相同的条件下利用一个变量来比较,同时还需要测量测量出分别在Fe3+和Cu2+的催化作用下,收集40mL气体的始、终时间,就能计算出反应速率。
(4)双氧水具有氧化性,能把亚铁离子氧化生成铁离子,反应的离子方程式是Fe2++2H2O2+4H+=Fe3++4H2O。
点点评:该题是中等难度的试题,试题综合性强,侧重对学生实验探究能力的培养,有利于激发学生的学习积极性,也有助于培养学生的规范实验设计能力。所以该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。该题能较好的考查学生实验设计、数据处理、图象分析的综合能力。在解答时注意已知信息的利用。
本题难度:一般