微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇.“绿色自由”构想技术流程如下:
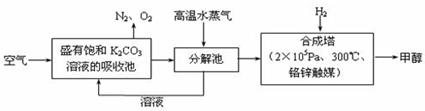
(1)在合成塔中,若有2.2kgCO2与足量H2恰好完全反应,生成气态的水和甲醇,可放出2473.5kJ的热量,试写出合成塔中发生反应的热化学方程式______.
(2)①上述合成反应具有一定的可逆性,从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300°C的温度,其原因是______.
②“绿色自由”构想技术流程中常包括物质和能量的“循环利用”,上述流程中能体现“循环利用”的除碳酸钾溶液外,还包括______.
③下列措施中能使n(CH3OH)/n(CO2)增大的是______.
A.升高温度? ? ?B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离? ?D.再充入1molCO2和3molH2
(3)甲醇可制作燃料电池.写出以氢氧化钾为电解质的甲醇燃料电池负极反应式______.当电子转移的物质的量为______时,参加反应的氧气的体积是6.72L(标准状况下).
(4)常温下,0.1mol/L?KHCO3溶液的pH大于8,则溶液中各种离子浓度由大到小的顺序为:______.
2、简答题 工业上生产硫酸时,将SO2氧化为SO3是关键一步.
(1)某温度下,2?SO2(g)+O2(g)?2SO3(g);△H=-196kJ?mol-1.开始时在10L的密闭容器中加入4.0mol?SO2(g)和5.0mol O2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=?.
(2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2,发生下列反应:2SO2(g)+O2(g)?2SO3(g)达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是?.
A.保持温度和容器体积不变,充入2mol?SO3
B.保持温度和容器体积不变,充入2mol?N2
C.保持温度和容器体积不变,充入0.5mol?SO2和0.25mol?O2
D.保持温度和容器内压强不变,充入1mol?SO3
E.升高温度?
F.移动活塞压缩气体
(3)某人设想以右上图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:?.
(4)在0.1mol?L-1的(NH4)2SO4溶液中,离子浓度由大到小的顺序是?.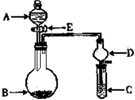
3、简答题 我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):
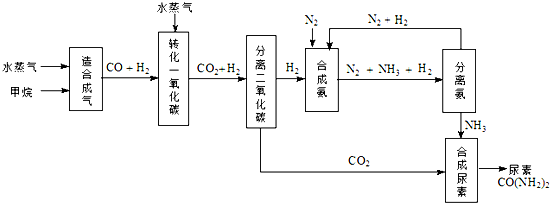
(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是______.
A、增大压强?B、升高温度?C、充入He气?D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
提高氢碳比[n(H2O)/n(CO)],K值______(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)______v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是______.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为______,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为______.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成______L?氨气.(假设体积均在标准状况下测定)
4、选择题 如图,向A充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a?L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述放热反应,X?(g)+Y(g)?

2Z(g)+W(g);?A保持恒压,B保持恒容,达平衡时,A的体积为1.4a?L.下列说法错误的是( )
A.反应速率:v(B)>v(A)
B.A容器中X的转化率为80%
C.平衡时的压强:PB>2PA
D.平衡时Y体积分数:A>B