|
|
|
���л�ѧ�ر�֪ʶ�㡶ԭ���ԭ�������⼼�ɣ�2017�����°棩(��)
2017-08-22 16:08:51
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������ҺΪ��������ˮ��Һ������ȼ�ϵ�ص�ⱥ��̼������Һһ��ʱ�䣬������ʱ�¶Ȳ������ö��Ե缫������˵����ȷ����
A����ص�������ӦʽΪ��O2ʮ2H2Oʮ4e-��4OH��
B������ظ�������mg����ʱ����������ͬʱ��mg��������
C������c(Na2CO3)��С
D�������c(KOH)���䣻��������ҺpH���
|
�ο��𰸣�A
���������ȼ�ϵ������������ԭ��Ӧ��A��ȷ������Ϊ�����ŵ磬������mg����ʱ����ת����m mol���ӣ���������Ϊ�����������ڷŵ磬��ʱ����m/4 mol��������8mg��B������ⱥ��̼������Һ��ʵ����ˮ��̼���Ƶ�Ũ�Ȳ��䣬C���������KOH��Ũ�ȱ�С��D����
���㣺����
����������������߿�����֪ʶ�㣬ע�ؿ���ѧ���������⡢���������������������������͵��ؽ��п��顣
�����Ѷȣ�һ��
2������� ij����A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ���� ��ˮ�ӳɵIJ���B��һ�ֳ��õ��л��ܼ���������������Ҫ��Ӧ�á�
��1��A�ĵ���ʽΪ________��B�ķ���ʽΪ________��
����B��O2�Ƴ�ȼ�ϵ�أ�����ϡ������ҺΪ�������Һ���ش�2��-��5���⣺
��2�������ϵĵ缫��ӦʽΪ_______________________________________��
��3�����ı�״���µ�5.6 L O2ʱ����__________mol���ӷ���ת�ơ�
��4����ʼ�ŵ�ʱ������������Һ��pH__________(���������С�����䡱)��
��5����Һ��H+��___________����__________���ƶ��������������������
�ο��𰸣���1��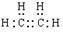 ������ʽ C2H6O ����1�֣� ������ʽ C2H6O ����1�֣�
��2��C2H6O -12e- +3H2O ��12H+ +2CO2 �� ��3�֣�?��3�� 1?��1�֣�
��4������ ��1�֣�?��5�� ����?���� �� ��1�֣�
�����������1��ij����A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����֪AΪ��ϩ�� ����ʽΪ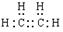 ����ˮ�ӳɵIJ���B��һ�ֳ��õ��л��ܼ�����BΪ�Ҵ������Ϊ����ʽ C2H6O �� ����ˮ�ӳɵIJ���B��һ�ֳ��õ��л��ܼ�����BΪ�Ҵ������Ϊ����ʽ C2H6O ��
��2������B��O2�Ƴ�ȼ�ϵ�أ�����ϡ������ҺΪ�������Һ�����Ҵ�ȼ�ϵ�ط�����������ԭ��Ӧ��֪�Ҵ�ʧȥ���ӣ����ڸ����Ϸ���ʧ���ӷ�ӦC2H6O -12e- +3H2O ��12H+ +2CO2 �� ����3�����ݵ����غ㣬������5.6 L O2ʱ����0.25mol������Ӧ�ˣ�ת��1mol���ӡ���4����ʼ�ŵ�ʱ��������Ӧ���������Ӳμ��˷�Ӧ���ʸ�����Һ��pH����5����Һ��H+�ɸ��������������ƶ���
�����Ѷȣ�һ��
3��ѡ���� ��A��B��C��D�Ŀ����Ƭ����������ʵ�飺
��A��B�õ���������ͬʱ����ϡH2SO4�У�A��Ϊ������
��C��D�õ���������ͬʱ����ϡH2SO4�У�������D�����ߡ�C��
��A��C�õ���������ͬʱ����ϡH2SO4�У�C�������������ݣ�
��B��D�õ���������ͬʱ����ϡH2SO4�У�D������������Ӧ���ݴ��ж����ֽ����Ļ��˳��Ϊ��?��
A��A>B>C>D?B��A>C>D>B
C��C>A>B>D?D��B>D>C>A
�ο��𰸣�B
���������������ϡH2SO4���ԭ��أ����ý���Ϊ������ʧȥ���ӷ���������Ӧ���ϲ����õĽ���Ϊ������H���������õ���������H2�����·�е������������ɸ����D�������������������������D��������������ԭ����У�A��B��ϡH2SO4ԭ��أ�AΪ������C��D��ϡH2SO4ԭ��أ�CΪ������A��C��ϡH2SO4ԭ��أ�AΪ������B��D��ϡH2SO4ԭ��أ�DΪ���������Ͽ�֪���������Ϊ��A>C>D>B��
�����Ѷȣ���
4������� ��18�֣�C��O��Na��Al��S��Cl�dz���������Ԫ��
��1��CԪ��λ��Ԫ�����ڱ��� ���ڣ��� �壻CԪ�ص�һ��ͬλ�ؿ��Բⶨ�������������ͬλ�صķ���Ϊ
��2���á����ڡ���С�ڡ����ڡ����
���Ӱ뾶
| ��ԭ��
| �õ�������
| N3- Al3+
| O2- S2-
| 35Cl 37Cl
|
��3����CaCO3������HCl��Һ��Ӧʱ��ÿ����4.4 g ���壨�����������ܽ⣩������a kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��������Ӧ���������ݳ���ȡ����������Һ������pH����������ε���̼������Һ�����pH�仯������ͼ��ʾ
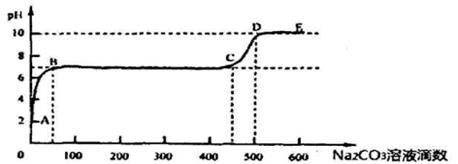

�������ӷ���ʽ��ʾB-C�η����ķ�Ӧ��
��4��������������������ȼ�ϵ�أ�д�������Ϊ����������Һʱ�����ϵĵ缫����ʽ
�ο��𰸣���1���� ��IVA �� 14C ��ÿ��1�֣���3�֣�
��2������ С�� ���ڣ�ÿ��1�֣���3�֣�
��3����CaCO3��s��+ 2HCl��aq��= CaCl2��aq��+ H2O(l) +CO2(g)?H =" -10a" kJ/mol ��2�֣�
��Ca2++ CO32-= CaCO3����2�֣�
��4��H2-2e-+2OH- = 2H2O��2�֣�
�����������1��CԪ��λ��Ԫ�����ڱ��ڶ����ڣ�IVA�壬����14C�ⶨ�������������ͬλ�صķ���Ϊ14C��
��2��N3-�� Al3+�ĵ��Ӳ�ṹ��ͬ����ԭ������С�����Ӱ뾶���������Ӱ뾶��N3-����Al3+��O�������Դ���S����O2-�Ļ�ԭ��С��S2-��35Cl�� 37Cl����ClԪ�صIJ�ͬԭ�ӣ���ѧ�������ƣ����Եõ���������ͬ��
��3����CaCO3������HCl��Һ��Ӧʱ���ɶ�����̼���壬�Ȼ��ơ�ˮ������4.4g������̼�����ʵ�����4.4g/44g/mol=0.1mol����1mol̼���������HCl��Һ��Ӧ�ų���������10akJ����÷�Ӧ���Ȼ�ѧ����ʽΪCaCO3��s��+ 2HCl��aq��= CaCl2��aq��+ H2O(l) +CO2(g)?H =" -10a" kJ/mol��
����Ϊ������̼������ˮ��ʹ�Ȼ�����Һ�����ԣ����Կ�ʼ�����̼�������ܽ�Ķ�����̼��Ӧ��BC�ε�pH���ֲ��䣬˵����ʱ�����̼�������Ȼ��Ʒ�Ӧ����̼��Ƴ��������ӷ���ʽΪCa2++ CO32-= CaCO3����
��4������ȼ�ϵ���и�������������Ӧ�������ڸ���������Ӧ�����������������Һ���������ƣ�������ʧȥ���ӣ���������Һ�е����������ӽ��Ϊˮ�����Ը����ĵ缫��ӦʽΪH2-2e-+2OH- = 2H2O��
���㣺����Ԫ��λ�õ��жϣ����Ӱ뾶����ԭ�Ե��жϣ��Ȼ�ѧ����ʽ����д��ԭ��ص缫��Ӧʽ����д
�����Ѷȣ�����
5������� �����8�֣�
ˮú�����Ƽ״��������̿�ͼ����
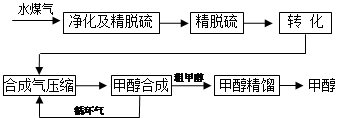
(ע:��ȥˮ�������ˮú����55��59%��H2��15��18%��CO��11��13%��CO2��������H2S��CH4����ȥH2S�ɲ��ô���Ǵ�ת����������CH4ת����CO���õ�CO��CO2��H2�Ļ�����壬������ĺϳɼ״�ԭ���������ɽ��м״��ϳ�)
��1����ˮú������Ҫ��ѧ��Ӧ����ʽΪ��C��s��+H2O��g�� CO��g��+H2��g�����˷�Ӧ�����ȷ�Ӧ���ٴ˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ??�� CO��g��+H2��g�����˷�Ӧ�����ȷ�Ӧ���ٴ˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ??��
�����������̼��ƽ��ת���ʵĴ�ʩ��??��
A������C��s��
B������H2O��g��
C�������¶�
D������ѹǿ
|
��2����CH4ת����CO����ҵ�ϳ����ô�ת���������䷴Ӧԭ��Ϊ��
CH4 (g)+3/2O2 (g)

CO (g)+2H2O (g) +519KJ����ҵ��Ҫѡ����ʵĴ������ֱ��X��Y��Z���ִ�����������ʵ�飨����������ͬ��
�� X��T1��ʱ��Ч����ߣ���ʹ����Ӧ���ʼӿ�Լ3��105����
�� Y��T2��ʱ��Ч����ߣ���ʹ����Ӧ���ʼӿ�Լ3��105����
�� Z��T3��ʱ��Ч����ߣ���ʹ�淴Ӧ���ʼӿ�Լ1��106����
��֪��T1��T2��T3������������Ϣ������Ϊ��������Ӧ��ѡ������˴�����
?���X����Y����Z������ѡ���������
?��
��3���ϳ�����ѹ�����º����10m3�״��ϳ������ڴ��������£����м״��ϳɣ���Ҫ��Ӧ�ǣ�2H2(g) + CO(g)

CH3OH(g)+181.6kJ��T4���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£����ܱ������м���CO��H2����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
����
| H2
| CO
| CH3OH
|
Ũ��/��mol��L��1��
| 0.2
| 0.1
| 0.4
|
�ٱȽϴ�ʱ�����淴Ӧ���ʵĴ�С��
v��
?v�棨�>������<������)��
��������ͬ�����CO��H2����T5�淴Ӧ��10 min��ﵽƽ�⣬��ʱc(H2)��0.4 mol��L��1��c(CO)��0.7 mol��L��1�����ʱ���ڷ�Ӧ����
v(CH3OH) ��
?mol��(L��min)��1��
��4�����������У��ϳ���Ҫ����ѭ������Ŀ����
?��
�ο��𰸣���1����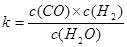 ��?��BC(2��)
��?��BC(2��)
��2��Z����Ч�ʸ��һ����¶ȵͣ�������Ը��ٶȿ죬��Ӧ�¶ȵͲ��ʸߣ�
��3���� >?��0.03 mol��L��1��min��1��
��4�����ԭ��CO��H2�������ʣ�����߲�����������ɣ���
�����������1����ƽ�ⳣ����ָ��һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����ƽ�ⳣ������ʽΪ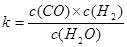 ��
��
��̼�ǹ��壬����̼������ƽ�ⲻ�ƶ�������ˮ������Ũ�ȣ�ƽ��������Ӧ�����ƶ���̼��ת������������Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���ת��������Ӧ���������ģ���������ѹǿ��ƽ�����淴Ӧ�����ƶ���ת���ʽ��ͣ�������ȷ�Ĵ�ѡBC��
��2�����ڷ�Ӧ�Ƿ��ȷ�Ӧ����Z��Ч�ʸ��һ����¶ȵͣ�����Ӧ��ѡ��Z��
��3���ٸ��ݱ������ݿ�֪����ʱ ��160����������Ӧ���ʴ����淴Ӧ���ʡ�
��160����������Ӧ���ʴ����淴Ӧ���ʡ�
����ͨ���������CO��ʧy�����ɼ״���Ũ����x����y��2x��0.4mol/L��y��x��0.7mol/L�����x��0.3mol/L����˼״��ķ�Ӧ������0.03 mol��L��1��min��1��
��4�����������У��ϳ���Ҫ����ѭ������Ŀ�������ԭ��CO��H2��������.
�����Ѷȣ�һ��


 CO (g)+2H2O (g) +519KJ����ҵ��Ҫѡ����ʵĴ������ֱ��X��Y��Z���ִ�����������ʵ�飨����������ͬ��
CO (g)+2H2O (g) +519KJ����ҵ��Ҫѡ����ʵĴ������ֱ��X��Y��Z���ִ�����������ʵ�飨����������ͬ�� CH3OH(g)+181.6kJ��T4���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£����ܱ������м���CO��H2����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
CH3OH(g)+181.6kJ��T4���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£����ܱ������м���CO��H2����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�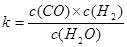 ��?��BC(2��)
��?��BC(2��)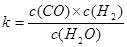 ��
�� ��160����������Ӧ���ʴ����淴Ӧ���ʡ�
��160����������Ӧ���ʴ����淴Ӧ���ʡ�