微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)下图是中学化学中一些常见的物质之间发生的一系列转化的框图(反应所需和所产生的水及某些反应条件已略),其中A、B、F、Y为黑色的固体,其中A、B、E、G、Y都含有同种VIA的元素,A和H、I含同种金属元素,但与H、I中该元素的化合价不同。E、G在常温常压下是气体,E有臭鸡蛋气味,G有刺激性气味。
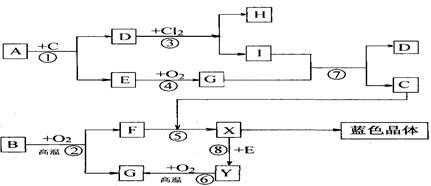
(1)写出下列物质的化学式:D____________,E____________。
(2)写出G通入I溶液发生反应⑦的离子方程式___________________________。
(3)以惰性电极电解X溶液的离子方程式_________________________________。
(4)试根据B、Y与氧气反应过程中的量的变化关系, 设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)
设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)
____________________________________________________________________
参考答案:(共11分)
(1)D为FeSO4(2分),E为H2S (2分)
(2)离子方程式2Fe3++SO2+2H2O=2Fe2++4H++SO42-(2分)
(3)离子方程式2Cu2++2H2O 2Cu+4H++O2↑(2分)
2Cu+4H++O2↑(2分)
(4)称一定 量的Cu2S和CuS充分燃烧,再称燃烧后的产物,若燃烧后的质量和反应物的质量相等,则被燃烧的物质是Cu2S,若燃烧后的质量比原来的反应物质量少,则被燃烧的物质是CuS。(3分)
量的Cu2S和CuS充分燃烧,再称燃烧后的产物,若燃烧后的质量和反应物的质量相等,则被燃烧的物质是Cu2S,若燃烧后的质量比原来的反应物质量少,则被燃烧的物质是CuS。(3分)
本题解析:略
本题难度:一般
2、填空题 已知:(1)A是XY型氧化物,它是黑色粉末;(2)将A和稀硫酸共热,得溶液B,向B中滴入适量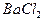 溶液,生成白色沉淀,过滤后得滤液C;(3)将C分成两份,在一份中加入烧碱溶液,可得蓝色絮状沉淀D;(4)往另一份C中放入一枚新铁钉,有单质E析出。已知A、B、C、D、E相互关系如图所示。
溶液,生成白色沉淀,过滤后得滤液C;(3)将C分成两份,在一份中加入烧碱溶液,可得蓝色絮状沉淀D;(4)往另一份C中放入一枚新铁钉,有单质E析出。已知A、B、C、D、E相互关系如图所示。
(1)写出A、B、C、D、E各物质的化学式:A__________,B__________,C__________,D__________,E__________。
(2)请写出上述反应中离子方程式。
? ?;
? ?;
参考答案:3Fe+2O2 Fe3O4? H2O
Fe3O4? H2O H2↑+O2↑
H2↑+O2↑
Fe+2HCl=FeCl2+H2? HCl+AgNO3=AgCl↓+HNO3
本题解析:略
本题难度:简单
3、推断题 中学化学常见的物质A、B、C、D之间存在如下图所示的转化关系。请按要求填空
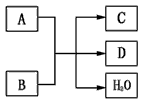
(1)若A是水垢和蛋壳的主要成分之一,B是厨房常见某调味品的一种成分,C常用于制作饮料,请写出该反应的离子方程式:______________ 。
(2)若A为黑色固体单质,C、D均能使石灰水变浑浊,则该反应的化学方程式为 _________________。
(3)若A为红色金属单质,该反应在常温下可以发生,无色气体C遇空气迅速变成红棕色,则产生1molC被氧化的A的物质的量为 ___________。
(4)若A为黑色粉末,C既能使品红溶液又能石蕊试液褪色,则反应中还原剂与氧化剂的物质的量之比为 _____________。
(5)若A为白色乳状物,其水溶液是实验室常用的检验试剂,D可作干燥剂,请写出此反应的化学方程式方程式__________________。
(6)若A为无色晶体,易分解,分解产物之一遇C产生大量白烟,则检验A中阳离子的方法是___________ 。
参考答案:(1)CaCO3+CH3COOH==Ca2++2CH3COO-+H2O +CO2↑
(2)C+2H2SO4(浓) CO2↑+2SO2↑+ 2H2O
CO2↑+2SO2↑+ 2H2O
(3)1.5 mol
(4)2:1
(5)2Ca(OH)2+2Cl2==Ca(ClO)2+CaCl2+ 2H2O
(6)取样于试管中,滴加NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,则证明原溶液中存在NH4+
本题解析:
本题难度:一般
4、填空题 已知(如图所示)①~④均为工业生产及应用中的常见反应.其中常温下B、D、J、P为气体,E为分子中原子个数之比为1:1的液体,M的焰色反应为黄色.A的相对分子质量为120,部分反应的产物已略去.
试回答下列问题:
(1)A的化学式为______;工业上反应①所用的设备名称是______.
(2)反应②的实验中,还需用到的药品是______、______(填药品名称).
(3)反应④的化学方程式为______,该反应装置中使用阳离子交换膜的作用是______.
(4)P与N反应的产物之一能和K的溶液发生反应,有红褐色沉淀生成.写出该产物与K以物质的量之比为1:2反应的离子方程式:______.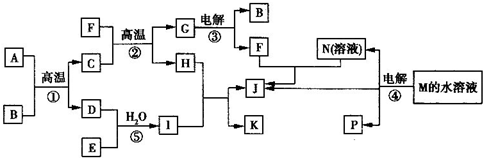
参考答案:高中阶段常见的工业生产有硫酸工业、合成氨工业、硝酸工业、硅酸盐工业.A的相对分子质量为120,且在高温下与B反应,推知反应①是硫酸工业中煅烧FeS2的反应,B、D为气体,所以A为FeS2,B为O2,C为Fe2O3,D为SO2,E为分子中原子个数之比为1:1的液体,能氧化SO2,故E为H2O2,I为H2SO4.Fe2O3在高温下与F(Al)发生铝热反应生成G(Al2O3)和H(Fe),电解熔融Al2O3得到O2、F(Al),Fe与H2SO4反应生成FeSO4与H2,J为气体,则K为FeSO4,J为H2.M的焰色反应为黄色,含有钠元素,电解产生三种物质N、P与H2,故M为NaCl,P为气体,则N为NaOH、P为Cl2.
(1)由上述分析可知,A为FeS2,工业上反应①所用的设备名称是沸腾炉,故答案为:FeS2;沸腾炉;
(2)反应②的实验是铝热反应,还需用到的药品是镁条、氯酸钾,故答案为:镁条;氯酸钾;
(3)反应④是电解饱和食盐水,化学方程式为:2NaCl+2H2O?通电?.?Cl2↑+H2↑+2NaOH;
由于生成的Cl2与H2相遇容易发生爆炸,且Cl2与NaOH溶液反应会导致氢氧化钠不纯,电解饱和食盐水使用阳离子交换膜阻止上述情况的发生,
故答案为:2NaCl+2H2O?通电?.?Cl2↑+H2↑+2NaOH;防止生成的Cl2与H2相遇容易发生爆炸,避免Cl2与NaOH溶液反应会导致氢氧化钠不纯;
(4)Cl2与NaOH溶液反应生成的NaClO具有强氧化性,将Fe2+氧化为Fe3+,从而生成Fe(OH)3沉淀,ClO-被还原为Cl-,再根据电荷守恒、电子转移守恒、原子守恒配平得:3ClO-+6Fe2++3H2O=2Fe(OH)3+4Fe3++3Cl-,
故答案为:3ClO-+6Fe2++3H2O=2Fe(OH)3+4Fe3++3Cl-.
本题解析:
本题难度:一般
5、填空题 A~L是由6种短周期元素且成的物质,各物质之间有如下转化关系:
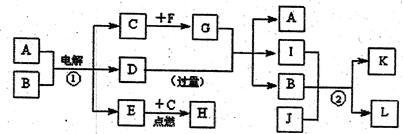
已知:
(a)C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b)J是能使澄清石灰水变浑浊的无色无味气体;
(c)化合物A、D、I、L的焰色反应显黄色;
(d)白色沉淀K既溶于H溶液,又能溶于D溶液;
(e)反应①是工业上生产D和C的重要方法
请回答下列问题:
(1)写出F的化学式:?,D的电子式:?
(2)写出下列有关反应的离子方程:
反应①:? ?;
?;
过量J与I反应:?
(3)G溶液呈?性(填“酸”、“碱”或“中”),请用离子方程式表示其原因: ?
参考答案:(1)Al?氢氧化钠的电子式?
(2)氯化钠溶液的电解和过量二氧化碳与偏铝酸钠溶液生成沉淀和碳酸氢钠离子方程式
(3)酸(这空1分,其余空都为2分)铝离子的水解离子方程式
本题解析:略
本题难度:一般