微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下列分子结构图中的

表示氢原子,

表示短周期的相邻的三种元素原子.小黑点表示没有形成共价键的最外层电子,短线表示共价键
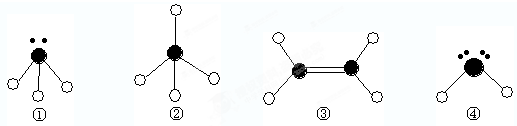
(1)以上分子中,中心原子采用sp2杂化的是______(填化学式);
(2)在③的分子中有______个σ键.在③与溴的四氯化碳溶液反应中,断裂的是③分子中的______键(填“σ”或“π”),形成的是______键(填“σ”或“π”).
(3)4种分子中,属于极性分子的是______(填序号,下同).键角由大到小的顺序是______,能结合质子(即H+)形成稳定离子的是______,形成______键(按电子对提供方式分类).
(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为:______.
参考答案:由结构模型可知①为NH3,②为CH4,③为C2H4,④为H2O或H2S,
(1)①为sp3杂化,②为sp3杂化,③为sp2杂化,④为sp3杂化,故答案为:C2H4;
(2)③为C2H4,含有5个δ键,C=C中有1个δ键,1个π键,π键不稳定,加成反应时易断裂,重新生成δ键,
故答案为:5;π;δ;
(3)①④结构部对称,属于极性分子,键角由大到小的顺序是③②①④,①④含有孤对电子,可形成配位键,
故答案为:①④;③②①④;①④;配位;
(4)①为NH3,可水的电离相似,则应存在2NH3?NH4++NH2-,故答案为:2NH3?NH4++NH2-.
本题解析:
本题难度:一般
2、选择题 下列可用氢键来解释的是?
A.浓的氢氟酸溶液中存在HF 和H2F
和H2F
B.SiH4沸点比CH4高
C.水和乙醇分别与金属钠反应,前者比后者剧烈
D.H2O比H2S稳定,前者1000℃以上才分解,后者300℃分解
参考答案:A
本题解析:原子半径小、吸引电子能力强的F、O、N与H原子间易形成氢键,氢键的存在可能会形成缔合物,影响物质的物理性质。B项中,因SiH4的相对分子质量比CH4的相对分子质量大,从而造成前者分子间作用力大,C、D两项均体现物质的化学性质,故只有A项成立。
本题难度:一般
3、选择题 在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是
[? ]
A.石墨的结构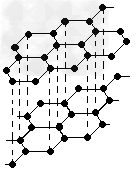
B.P4的结构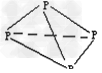
C.CCl4的结构
D.立方烷的结构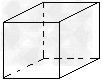
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列化学用语表达正确的是
[? ]
A.乙酸的分子式:CH3-COOH
B.丙烷分子的球棍模型:
C.Ar原子的结构示意图: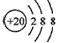
D.四氯化碳的电子式: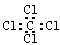
参考答案:B
本题解析:
本题难度:简单
5、选择题 X、Y、Z和W为原子序数依次增大的四种短周期元素.已知:①在元素周期表中,Z与X、W直接相邻;②X、Z和W三种元素原子最外层电子数之和为19,Y为同周期中原子半径最小.下列各选项正确的是( )
A.离子的还原性:Z<Y
B.水溶液的酸性:HY>HW
C.漂白作用:WX2>HWX
D.与水反应:Y2+H2O?HY+HYO
参考答案:X、Y、Z和W为原子序数依次增大的四种短周期元素.Z与X的原子序数相差≥2,在元素周期表中,Z与X、W直接相邻,则Z、X不可能处于同一周期,故X、Z处于同族,X、Z和W三种元素原子最外层电子数之和为19,所以Z、X、W不可能处于同族,故Z、W处于同一周期,令Z、X的最外层电子数为a,则W的最外层电子数为a+1,所以a+a+a+1=19,解得a=6,故X为氧元素,Z为硫元素,W为氯元素.Y的原子序数介于氧元素与硫元素之间,Y为同周期中原子半径最小,故Y为氟元素.
A、元素非金属性越强,相应阴离子的还原性越弱,F元素的金属性可能比S元素强,故Y阴离子的还原性可能比S2-弱,故A错误;
B、Y为F元素、W为氯元素,氢氟酸为弱酸,盐酸为强酸,故B错误;
C、W为氯元素,ClO2的氧化能力大于HClO,所以漂白能力ClO2>HClO,故C正确;
D、氟气与水反应生成氢氟酸与氧气,故D错误.
故选:C.
本题解析:
本题难度:一般