|
高考化学试题《常见的化学电源》在线测试(2017年最新版)(六)
2017-08-22 16:27:55
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 甲烷燃料电池(电解质是KOH溶液)的总反应为:CH4+2KOH+2O2=K2CO3+3H2O.?下列有关的说法中不正确的是( )
A.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
B.该燃料电池在使用过程中电解质溶液的浓度和性质均发生变化
C.负极反应式:CH4+3H2O-8e-=CO32-+7H+
D.正极反应式:2O2+4H2O+8e-=8OH-
参考答案:A、在燃料电池工作时,化学能大多数转化为电能,甲烷燃烧伴随着光能和热能,甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大,故A正确;
B、燃料电池在使用过程中发生电池反应:CH4+2KOH+2O2=K2CO3+3H2O,电解质氢氧化钾被消耗,生成碳酸钾溶液,电解质溶液的浓度和性质均发生变化,故B正确;
C、甲烷燃料电池,具有还原性的甲烷为原电池的负极,发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,故C错误;
D、通入氧气的一极为原电池的正极,发生还原反应,电极反应式为2O2+4H2O+8e-=8OH-,故D正确.
故选C.
本题解析:
本题难度:简单
2、选择题 下图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池 (MH-Ni碱性电池)。下列有关说法不正确的是

A.放电时正极反应为:NiOOH+H2O+e-=Ni(OH)2+OH-
B.放电时负极反应为:MH+OH
|
参考答案:
本题解析:
本题难度:一般
3、选择题 目前人们掌握了可充电锌―空气电池技术,使这种电池有了更广泛的用途。这种电池使用特殊技术吸附空气中的氧,以苛性钠为电解质,电池放电时的总反应为2Zn+O2 2ZnO,下列判断正确的是( ) 2ZnO,下列判断正确的是( )
A.放电时,OH-向负极方向移动
B.放电时,正极反应式为Zn+2OH--2e- ZnO+H2O ZnO+H2O
C.充电时,Zn发生氧化反应
D.充电时,阴极反应为O2+2H2O+4e- 4OH- 4OH-
参考答案:A
本题解析:原电池放电时阴离子移向负极,阳离子移向正极,A项正确;该原电池中Zn为负极,其正极反应式为O2+4e-+2H2O 4OH-,B项错误;充电时,ZnO发生还原反应,OH-发生氧化反应,C项错误;充电时阴极反应式应为ZnO+H2O+2e- 4OH-,B项错误;充电时,ZnO发生还原反应,OH-发生氧化反应,C项错误;充电时阴极反应式应为ZnO+H2O+2e- Zn+2OH-,D项错误。 Zn+2OH-,D项错误。
本题难度:一般
4、填空题 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,其构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。
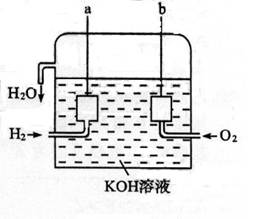
⑴a极是?,电极反应式是?。
⑵b极是?,电极反应式是?。
⑶氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出甲烷燃料电池中a极的电极反应式为?。此时电池内的总反应方程式为?。
参考答案:⑴负极,2H2+4OH-→4H2O+4e-;⑵正极,O2 + 2H2O + 4e-→ 4OH-;⑶CH4+10OH-= CO32-+ 7H2O + 8 e-,CH4+2O2+2KOH = K2CO3?+? 7H2O 。
本题解析:依据燃料电池的电极及电极反应可知a、b两极各是什么极及其电极反应式。又由于甲烷燃烧生成二氧化碳,但在KOH溶液中应生成碳酸根离子,又碳元素的化合价由-4升到+4,故1mol的甲烷应失去8mol的电子,即电极反应式为:CH4+10OH-= CO32-+ 7H2O + 8 e-。
本题难度:一般
5、选择题 高铁电池是一种新型碱性可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O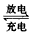 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
[? ]
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
参考答案:C
本题解析:
本题难度:一般
|