| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ��������ԭ���ԭ������Ƶ����ǿ����ϰ��2017�����°棩(��)
�ο��𰸣�D ���������������Ӧ��PbSO4������ԭ��Ӧ,����Pb,A�����;�ŵ������Li+�������ƶ�,B�����;�ɵ���ܷ�Ӧʽ��֪,ÿת��0.1 mol����,����������0.05 mol Pb,����Ϊ10.35 g,C�����;������,����ʲ�������̬,���Ӳ��������ƶ�,���ܵ���,������ӵ������������,ָ�벻ƫת,D����ȷ�� �����Ѷȣ�һ�� 4��ѡ���� ijԭ���װ����ͼ��ʾ�������й������У���ȷ���ǣ������� |
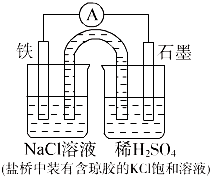
�ο��𰸣�D
���������
�����Ѷȣ���
5������� ��14�֣����û�ѧ��Ӧԭ�����������������
��1����֪�� ��CO(g)+2H2(g)  CH3OH(g) ��Hl= ��91kJ��mol��l
CH3OH(g) ��Hl= ��91kJ��mol��l
��2CH3OH(g) CH3OCH3(g)+H2O(g) ��H2= ��24 kJ��mol��l ��CO(g) +H2O(g)
CH3OCH3(g)+H2O(g) ��H2= ��24 kJ��mol��l ��CO(g) +H2O(g)  CO2(g)+H2(g) ��H3= ��41 kJ��mol��l
CO2(g)+H2(g) ��H3= ��41 kJ��mol��l
��������Ӧ��ƽ�ⳣ������ΪK1��K2��K3 ��Ӧ 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) ��H= .
��Ӧ 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) ��H= .
��ѧƽ�ⳣ��K= ���ú�K1��K2��K3�Ĵ���ʽ��ʾ����
��2��һ�������£����������Ϊ1:2��CO��H2����ͨ�����һ�����ܱ������з�����Ӧ 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g)��������˵����Ӧ�ﵽƽ��״̬�� ��
3CO(g) +3H2(g) CH3OCH3(g) +CO2(g)��������˵����Ӧ�ﵽƽ��״̬�� ��
a����ϵѹǿ���ֲ��� B����������ܶȱ��ֲ���
c�� CO��H2�����ʵ������ֲ��� d��CO�������ٶȵ���CO2����������
��3����������ˮ�õ���ˮ����25���£���x mol��L��l�İ�ˮ��y mol��L��1������������ϣ���Ӧ����Һ�����ԣ���c(NH4+)____c��Cl�������>������<������=�������ú�x��y�Ĵ���ʽ��ʾ����ˮ�ĵ���ƽ�ⳣ�� .
��4����ѧ�ҷ�����ʹNH3ֱ������ȼ�ϵ�صķ�������װ���ò������缫������������Һ�У�һ���缫ͨ���������һ�缫ͨ��NH3�����ط�ӦʽΪ��4NH3+3O2 = 2N2+6H2O���������ҺӦ�� ������ԡ��������ԡ��������ԡ�����
д�������ĵ缫��Ӧ����ʽ .
�ο��𰸣���ÿ��2�֣���14�֣�
(1)-247KJ��mol����������K12��K2��K3
(2)a��c
(3) = K= mol��L-1
mol��L-1
(4)���� O2+2H2O+4e����4OH��
�����������1�����ݸ�˹���ɵ�3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) ��H=�١�2+��+��=��Hl��2+��H2+��H3=-247KJ��mol������ƽ�ⳣ��K= K12��K2��K3
CH3OCH3(g) +CO2(g) ��H=�١�2+��+��=��Hl��2+��H2+��H3=-247KJ��mol������ƽ�ⳣ��K= K12��K2��K3
��2��a����������̶���3CO(g) +3H2(g) CH3OCH3(g) +CO2(g)�Ƿ�Ӧǰ������ѹǿ�����ı�Ŀ��淴Ӧ��������ϵѹǿ���ֲ���ʱ��ƽ��״̬����ȷ��b����������̶������������غ㶨�ɣ���������ܶ�ʼ�ղ��䣬���Բ�����Ϊƽ��״̬����ı�־������c����Ӧ��ʼʱ��CO��H2�����ʵ���һֱ���٣���CO��H2�����ʵ������ֲ��䣬���ټ���ʱ֤���Ѵ�ƽ��״̬����ȷ��d��CO�����������κ�״̬��������CO2���������ʣ�����ѡac��
CH3OCH3(g) +CO2(g)�Ƿ�Ӧǰ������ѹǿ�����ı�Ŀ��淴Ӧ��������ϵѹǿ���ֲ���ʱ��ƽ��״̬����ȷ��b����������̶������������غ㶨�ɣ���������ܶ�ʼ�ղ��䣬���Բ�����Ϊƽ��״̬����ı�־������c����Ӧ��ʼʱ��CO��H2�����ʵ���һֱ���٣���CO��H2�����ʵ������ֲ��䣬���ټ���ʱ֤���Ѵ�ƽ��״̬����ȷ��d��CO�����������κ�״̬��������CO2���������ʣ�����ѡac��
��3�����ݵ���غ㶨�ɣ������백ˮ��Ϻ����Һ�����ԣ���c(H��)=c��OH������c(Cl-)+ c��OH����=c(NH4+)+c(H��)������c(Cl-)=c(NH4+)����25���£�������Һ��c(H��)= c��OH����=1��10-7mol/L���������백ˮ��Ũ����ȣ���������Ϻ������Ȼ����Һ�����ԣ���ʵ����Һ�����ԣ�˵����ˮ��Ũ�ȴ��������Ũ�ȣ���ˮ����������ߵ������Ϊ1L�������ᷴӦ��ʣ�ఱˮ�����ʵ�����x-y��mol��һˮ�ϰ���Ũ��Ϊ��x-y��/2mol/L��c(NH4+)=c(Cl-)=y/2mol/L����ˮ�ĵ���ƽ�ⳣ��K= c��OH����c(NH4+)/ c(NH3��H2O)= 1��10-7mol/L��y/2mol/L/��x-y��/2mol/L= mol��L-1��
mol��L-1��
��4�����ݵ�ط�ӦʽΪ��4NH3+3O2 =2N2+6H2O���жϰ�������������Ӧ������������ԭ��Ӧ������ʧ���ӳ�Ϊ�����������ӣ����Ե������ҺӦ�Լ��ԣ������в�������ˮ����Ϊ�������ҺΪ���ԣ����������������Ļ�ԭ��Ӧ�������õ�����ˮ����������������ӣ��缫��ӦʽΪO2+2H2O+4e����4OH��
���㣺�����˹���ɵ�Ӧ�� ����ѧƽ��״̬���жϣ���ѧƽ�ⳣ���ļ��㣬ԭ��ط�Ӧԭ����Ӧ��
�����Ѷȣ�����
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶�ȼ��仯��.. | |
| �����Ŀ |