微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:N2(g)+3H2(g) 2NH3(l) △H=" -132" kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
2NH3(l) △H=" -132" kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
| H2(g)
| N2(g)
| NH3(g)
|
1mol分子中的化学键形成时要释放出的能量/kJ
| 436
| 946
| a
|
一定条件下,在体积1L的密闭容器中加入1molN2(g)和3molH2(g)充分反应,生成NH3(g)放出热量QkJ,

下列说法正确的是
A.上图可表示合成氨过程中的能量变化
B.a的数值为1173
C.Q的数值为92
D.其它条件相同,反应使用催化剂时释放出的能量大于无催化剂时释放出的能量
参考答案:B
本题解析:A、反应是放热反应,反应物能量应高于生成物,故A错误;B、△H=反应物键能和-生成物键能和,有-132KJ/mol+40KJ/mol=946KJ/mol+3×436KJ/mol-6aKJ/mol,a=391KJ/mol,1mol氨气含有3molN-H键,故B正确;C、蒸发1mol NH3(l)需要吸收的能量为20kJ,N2(g)+3H2(g) 2NH3(l)△H=-132kJ/mol,2NH3(l)=2NH3(g)△H=+40KJ/mol,据盖斯定律可得:N2(g)+3H2(g)
2NH3(l)△H=-132kJ/mol,2NH3(l)=2NH3(g)△H=+40KJ/mol,据盖斯定律可得:N2(g)+3H2(g) 2NH3(g)△H=-92kJ/mol,1molN2(g)和3molH2(g)充分反应,但不能完全反应,所以Q<92,故C错误;D、催化剂只能加快反应速率,不影响反应热的大小,故D错误;故选B。
2NH3(g)△H=-92kJ/mol,1molN2(g)和3molH2(g)充分反应,但不能完全反应,所以Q<92,故C错误;D、催化剂只能加快反应速率,不影响反应热的大小,故D错误;故选B。
考点:考查放热反应的图象、利用键能求算反应热、可逆反应的反应热、盖斯定律的应用等
本题难度:一般
2、选择题 下列既有极性键,又有非极性键的非极性分子是 (?)
A.二氧化硫
B.四氯化碳
C.过氧化氢
D.乙炔
参考答案:D
本题解析:不同种非金属元素之间形成的化学键是极性键,同一种非金属元素之间形成的化学键是非极性键,据此可知,A、B中只有极性键。C是极性分子,不正确,答案选D。
点评:该题是中等难度的试题,试题难易适中,侧重对学生能力的培养。该题的关键是明确极性键、非极性键以及极性分子和非极性分子的判断标准,并能结合题意灵活运用即可。
本题难度:简单
3、选择题 共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量。如H―H键的键能是436KJ/mol,是指1molH2分子变成2molH原子需要吸收436KJ的能量。你认为下列分子中的共价键能量最大的是( )
?
A.HF
B.HCl
C.HBr
D.HI
参考答案:?
本题解析:可通过比较成键原子半径的大小得出键能的大小。一般来说,成键原子半径越小,键长越短,键能越大。
本题难度:一般
4、填空题 (1)已知热化学方程式如下:N2(g)+3H2O(1)==2NH3(g)+ O2(g);△H="+765.2" kJ・mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
O2(g);△H="+765.2" kJ・mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
(2)明矾能净水的原因: (用离子方程式和必要的文字解释)
___________________________________________________________________________。
(3)已知FeCl3能水解 ,则配制FeCl3溶液的方法是 ____ 。
(4)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
铁锅的锈蚀是 腐蚀(填“析氢”或“吸氧”)
写出铁锅腐蚀负极的电极反应式:
正极的电极反应式:
参考答案:(1) 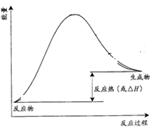 (2分);
(2分);
(2)因为明矾溶于水发生Al3++3H2O Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质。(2分)
Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质。(2分)
(3)将FeCl3固体溶解在浓盐酸中,再加水稀释至所需浓度。(2分)
(4)吸氧腐蚀(1分),2Fe-4e-=2Fe2+(2分), O2 + 2H2O + 4e-= 4OH-(2分)
本题解析:(1)根据反应的热化学方程式可知,该反应是吸热反应,所以反应物的总能量低于生成物的总能量,则图像是(见答案)。
(2)因为明矾溶于水电离出的铝离子发生水解反应,Al3++3H2O Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质,所以明矾可以作为净水剂。
Al(OH)3+3H+,生成Al(OH)3胶体能吸附水中的悬浮物质,所以明矾可以作为净水剂。
(3)FeCl3能水解,溶液显酸性,所以配制FeCl3溶液的方法是将FeCl3固体溶解在浓盐酸中,再加水稀释至所需浓度。
(4)钢铁的腐蚀主要是吸氧腐蚀,其中负极是铁失去电子,电极反应式是2Fe-4e-=2Fe2+。正极是氧气得到电子,则电极反应式是O2 + 2H2O + 4e-= 4OH-。
考点:考查化学反应中的能量变化、明矾净水、氯化铁的配制以及钢铁的吸氧腐蚀
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,基础性强,侧重对学生基础知识的巩固与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范答题能力。
本题难度:一般
5、填空题 ①Ar ②CO2 ③KCl ?④NaOH四种物质中,只存在共价键的是?,(填序号,下同)只存在离子键的是?,既存在离子键,又存在共价键的是?,不存在化学键的是?。
参考答案:②;③;④;①
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。稀有气体元素的最外层电子已经达到稳定结构,所以稀有气体分子中不存在化学键。
本题难度:一般