微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式中,正确的是(?)
A.小苏打与烧碱溶液反应: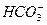 +OH-====CO2↑+H2O
+OH-====CO2↑+H2O
B.金属钾与水的反应:2K+2H2O====2K++2OH-+H2↑
C.钾与硫酸铜溶液的反应:2K+Cu2++2H2O====Cu(OH)2↓+2K++H2↑
D.碳酸钡溶于盐酸中: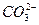 +2H+====CO2↑+H2O
+2H+====CO2↑+H2O
参考答案:BC
本题解析: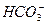 与OH-发生如下反应:
与OH-发生如下反应: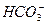 +OH-====H2O+
+OH-====H2O+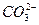 。A选项不正确。B选项正确。钾放入CuSO4(aq)中,先后发生下列两个反应:
。A选项不正确。B选项正确。钾放入CuSO4(aq)中,先后发生下列两个反应:
2K+2H2O====2KOH+H2↑;2KOH+CuSO4====Cu(OH)2↓+K2SO4,其总反应方程式和离子方程式分别为:
2K+2H2O+CuSO4====Cu(OH)2↓+K2SO4+H2↑
2K+2H2O+Cu2+====Cu(OH)2↓+2K++H2↑
C选项正确。碳酸钡难溶于水,应用化学式表示。D选项不正确。
本题难度:简单
2、计算题 在密闭容器上,放入碳酸铵和氢氧化钠固体共A克,将容器加热至200℃,经充分反应后,排出其中的气体,冷却称得剩余固体的质量为B克。问容器内碳酸铵和氢氧化钠各多少克?
参考答案:
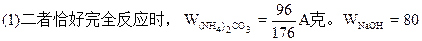
/176A克;
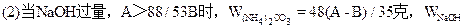
=(48B-13A)/35克;
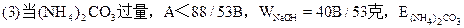
=A-40B/53克。
本题解析:可能发生如下反应:
(NH4)2CO3+2NaOH 2NH3↑+Na2CO3 ?①
2NH3↑+Na2CO3 ?①
(NH4)2CO3 2NH3↑+CO2↑+H2O↑?②
2NH3↑+CO2↑+H2O↑?②
在加热过程中应首先发生反应①,只有当(NH4)2CO3过量时才能继续发生反应②。并由以上反应可看出,NaOH过量时减重少。下面分别讨论。
(1)当二者恰好反应时:
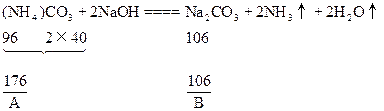
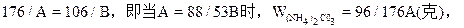
WNaOH=80/176A(克),(也可用B表示)。
(2)当NaOH过量,A>88/53B时,只发生反应①。先计算。(NH4)2CO3的量。
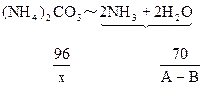
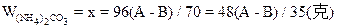
WNaOH=A-48(A-B)/53=(48B-13A)/35(克)
(3)当(NH4)2CO3过量,A<88/35B时,发生反应①、②。
但由②知(NH4)2CO3全分解无固体剩余,所以还由①式计算,先求NaOH的量。
2NaOH~Na2CO3
∴WNaOH=y=80B/106=40B/53(克),
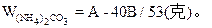
本题难度:一般
3、选择题 为了验证NaHCO3固体中是否含有Na2CO3?,下列实验及判 断中,正确的是(?)
A.加热,观察是否有气体放出
B.溶于水后加BaC12,看有无沉淀
C.溶于水后加石灰水,看有无沉淀
2,4,6
D.取固体变色试样加盐酸,看是否有气泡产生
参考答案:B
本题解析:略
本题难度:简单
4、推断题 物质的转化关系如图所示(有的反应可能在水溶液中进行,有的反应中反应物和生成物未全部给出,反应条件也未注明),其中甲可由 两种单质直接化合得到,乙为金属单质,F的溶液中只含一种溶质,G 为酸,乙在G的浓溶液中发生钝化。
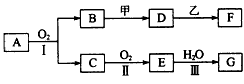
(1)若甲是既有离子键又含有非极性共价键的淡黄色固体化合物,化合物A所含的电子数与Ne原子相同。
①1.7g A与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式。
_____________________
②写出B与甲反应的化学方程式。_____________________
③写出D与乙反应的离子方程式。_____________________
(2)若乙的基态原子外围电子排布式为3d64s2,A为含有乙元素的化合物,框图中的甲改为甲的溶液。
①写出D溶液中金属离子基态时外围电子排布式_____________________
②说明C转化为E的反应条件_____________________
参考答案:
(1)①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -906.8kJ/mol;②2Na2O2+2H2O=4NaOH+O2↑;③2Al+2H2O+2OH-=2AlO2-+3H2↑
(2)①3d5;②常压、加热、催化剂
本题解析:
本题难度:一般
5、填空题 (10分)钠和铝是两种重要的金属。请回答:
(1)钠元素的金属性比铝的?(填“强”或“弱”);常温下,可用?(填“钠”或“铝”)制成的容器盛装浓硫酸或浓硝酸。
(2)将一小块金属钠投入水中,发生反应的化学方程式为?;可观察到的实验现象是?(填序号)。
a.钠沉到水底? b.钠熔成小球? c.小球四处游动
(3)铝与氢氧化钠溶液反应的离子方程式为?。
参考答案:(1)强?铝?(2)2Na? +? 2H2O? ="?" 2NaOH? + H2 ↑
b c? (3)2Al+2OH-+2H2O==2AlO2- +? 3H2↑
本题解析:略
本题难度:一般