| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《弱电解质电离平衡》考点强化练习(2017年押题版)(十)
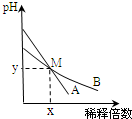 参考答案:A、稀释前,c(AOH)=0.1mol/L,c(BOH)>0.01mol/L,则c(AOH)<10c(BOH),故A错误; 本题解析: 本题难度:一般 5、填空题 (6分)室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
(2)以下各空均选填“>、<、=”。 实验②反应后的溶液中:c(A-)+c(HA) 0.1mol・L-1 室温下,将pH=3的HA溶液稀释到原体积的10倍后,溶液的pH 4 室温时,向等体积pH=a的盐酸和pH=b的HA溶液中分别加入等量的氢氧化钠后,两溶液来源:91考试网 91exam.org均呈中性,则a b 参考答案:(3)20 mL 0.1 mol/L NaA溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中离子浓度由大到小的顺序是 。(1) HA 本题解析: 本题难度:困难 | |||||||||||||||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《硫及其化合物》高.. | |