微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于所有的化学平衡体系,采取下列措施,一定会使平衡发生移动的是( )
A.改变温度
B.增大压强
C.改变浓度
D.使用催化剂
参考答案:A.任何化学反应一定伴随能量的变化,升高温度,化学平衡向着吸热方向进行,降低温度平衡向放热反应方向移动,故A正确;
B.对于没有气体参加的反应,或是前后气体体积不变的反应,压强不会引起平衡的移动,故B错误;
C.对于反应前后气体体积不变的反应,同等程度改变反应混合物各组分的浓度,平衡不移动,故C错误;
D.使用催化剂只能改变化学反应的速率,不会引起化学平衡的移动,故D错误.
故选C.
本题解析:
本题难度:简单
2、推断题 甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
(Ⅰ)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B 的浓溶液后,相互靠近会看到白烟;
(Ⅱ)各物质之间存在如下图所示的转化关系:

请回答下列问题:
(1)C溶液显____(填“酸”“碱”或“中”)性,若A溶液的物质的量浓度是B溶液的物质的量浓度的2倍,则等体积混合后溶液中各离子浓度由大到小的顺序为____________(用离子符号表示)。
(2)一定条件下,乙气体与甲气体充分反应生成6.8 g A气体,可放出18.44 kJ热量,则该反应的热化学方程式为____________________
(3)在一定温度下,向容积不变(容积为10 L)的密闭容器中加入2 mol乙气体、8 mol甲气体及固体催化剂。10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,用乙气体表示的反应速率为:
________,反应达平衡状态时甲气体的转化率为________,若想提高A的产率,根据化学平衡移动原理,请提出合理的建议:____________(任意写一条)。在上述平衡中,若再加入2 molA气体、2 mol乙气体,则此时化学平衡将________(填“向正方向”“向逆方向” 或“不”)移动。
(4)白色沉淀M可溶于A的水溶液,这与AgOH溶于A的水溶液类似,写出该反应的离子方程式_________。
参考答案:(1)酸;c(NH4+) >c(Cl-)>c(OH-)>c(H+)
(2)N2(g)+3H2(g)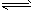 2NH3(g); △H= -92.2 kJ/mol
2NH3(g); △H= -92.2 kJ/mol
(3)0.01 moL/(L・min);37.5%;增大氢气浓度或增大氮气浓度(或增大反应物浓度)或及时移出氨气或降低温度或增大压强;向逆方向
(4)AgCl+2NH3・H2O==Ag(NH3)2++Cl-+2H2O
本题解析:
本题难度:一般
3、选择题 一定温度下,向一个一定容积的密闭容器中放入2molX和3molY,发生反应:X(气)+Y(气)?mZ(气)+nR(气),达平衡时,Z的体积分数为φ1,维持温度不变,若把3molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,则φ1与φ?2的关系为( )
A.φ1>φ2
B.φ1<φ2
C.φ1=φ2
D.无法判断
参考答案:密闭容器中放入2molX和3molY,发生反应:X(气)+Y(气)?mZ(气)+nR(气),达平衡时,Z的体积分数为φ1;维持温度不变,若把3molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,x和y这两种气体的反应比为1:1,达到平衡时参与反应的量取决于最小者,即2molx和2moly反应生成z,生成的Z的量是相同的,容器体积不变,Z的条件分数相同;
故选C.
本题解析:
本题难度:一般
4、简答题 如图所示,在一定温度下,把2体积N2和6体积H2通入一个带有活塞的容积可变的容器中,活塞的一端与大气相通,容器中发生以下反应:N2+3H2?2NH3(正反应放热),若反应达到平衡后,测得混合气体的体积为7体积.据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:
①若a=1,c=2,则b=______.在此情况下,反应起始时将向______(填“正”或“逆”)反应方向进行.
②若需规定起始时反应向逆反应方向进行,则c的取值范围是______.
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是______,原因是______.
参考答案:(1)①反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同,恒温恒压条件下,采用极限分析法,c体积的氨气完全转化为氮气和氧气之比是1:3,所以只要a:b=2:6,则b=3a=3,因反应前混合气体为8体积,反应后混合气体为7体积,体积差为1体积,由差量法可解出平衡时氨气为1体积;而在起始时,氨气的体积为c=2体积,比平衡状态时大,为达到同一平衡状态,氨的体积必须减小,所以平衡逆向移动,
故答案为:3;逆;
②若让反应逆向进行,由上述①所求出的平衡时氨气的体积为1可知,氨气的体积必须大于1,最大值则为2体积氮气和6体积氢气完全反应时产生的氨气的体积,即为4体积,则1<c≤4,
故答案为:1<c≤4;
(2)由6.5<7可知,上述平衡应向体积缩小的方向移动,即向放热方向移动,所以采取降温措施,
故答案为:降低温度、降低温度平衡向正反应方向移动,气体总分子数减少.
本题解析:
本题难度:一般
5、选择题 投入一定量的物质A和B发生可逆反应:2A(g)+nB(g) mC(g)?,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如图所示,?有关该反应的说法正确的是
mC(g)?,在温度分别为T1、T2,压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如图所示,?有关该反应的说法正确的是
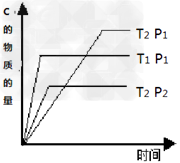
[? ]
A.?n+2<m?该反应正反应为放热反应
A.?n+2<m?该反应正反应为吸热反应
C.?n+2>m?该反应正反应为放热反应
D.?n+2>m?该反应正反应为吸热反应
参考答案:A
本题解析:
本题难度:一般