|
���л�ѧ֪ʶ�㽲�⡶���ܵ���ʵ��ܽ�ƽ�⡷������ѵ��2017���̰棩(��)
2017-08-26 00:33:28
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵���У���ȷ����
A�����ܵ������ˮ��Һ�дﵽ�����ܽ�ƽ��ʱ���������ܽ⼴ֹͣ
B��KspԽС�����ܵ������ˮ�е��ܽ�����һ��Խ��
C��Ksp�Ĵ�С������Ũ���أ�ֻ�����ܵ���ʵ����ʺ��¶��й�
D����ͬ�¶��£� AgCl��ˮ�е��ܽ���������NaCl��Һ�е���ͬ
�ο��𰸣�C
���������
��ȷ�𰸣�C
A������ȷ�����ܵ������ˮ��Һ�дﵽ�����ܽ�ƽ��ʱ���������ܽ����ڽ��У�ֻ�dz������ʵ����ܽ����ʣ�
B������ȷ�������ʵ��������ʱ��KspԽС�����ܵ������ˮ�е��ܽ�����һ��Խ����
C����ȷ��
D������ȷ����ͬ�¶��£� AgCl��ˮ�е��ܽ���������NaCl��Һ�д�NaCl��Һ��Cl�DŨ�ȴ�����AgCl�ܽ⡣
�����Ѷȣ���
2��ѡ���� ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��
��֪��p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)������˵����ȷ����
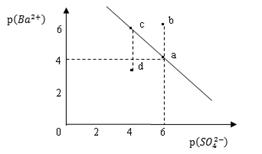
A�����¶��£�Ksp (BaSO4 )=1.0��10��24
B��a���Ksp (BaSO4 )��b���Ksp (BaSO4 )
C��d���ʾ���Ǹ��¶���BaSO4�IJ�������Һ
D������BaCl2����ʹ��Һ�� c��䵽a��
|
�ο��𰸣�D
���������A�����ᱵ���������������Ӻͱ����ӣ�a��ʱp(Ba2+)=-lgc(Ba2+)=4����c(Ba2+)=10-4mol/L��p(SO42-)=-lgc(SO42-)=6����c(SO42-)=10-6mol/L�����Ը��¶��£�Ksp (BaSO4 )= c(Ba2+) c(SO42-)=1.0��10��10������B���¶���ͬ�����ᱵ���ܶȻ���ͬ������C����Ϊp(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)�Ǽ���������ֵԽС�����Ӧ������Ũ��Խ������d��ʱc(Ba2+) c(SO42-)>1.0��10��10������ҺΪ��������Һ������D��c��ʱ�����Ȼ�����Һ������Һ�еı�����Ũ������p(Ba2+)��С�����ܽ�ƽ�������ƶ������������Ũ�ȼ�С��p(SO42-)������c��䵽a�㣬��ȷ����ѡD��
���㣺����Գ����ܽ�ƽ��ͼ��ķ����ж�
�����Ѷȣ�һ��
3������� ��8�֣�������ͭ����Һ�д�������ƽ�⣺Cu��OH��2��s��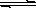 Cu2����aq����2OH����aq������������Ksp��c��Cu2������ c2��OH������2��10��20mol2��L��2�� Cu2����aq����2OH����aq������������Ksp��c��Cu2������ c2��OH������2��10��20mol2��L��2��
��1��ij����ͭ��Һ��c��Cu2������0.02mol/L����Ҫ����Cu��OH��2������Ӧ������ҺpHʹ֮������������������
��2��Ҫʹ0.2mol/L����ͭ��Һ��Cu2��������Ϊ��ȫ��ʹCu2��Ũ�Ƚ���ԭ����ǧ��֮һ������Ӧ����Һ���������������Һʹ��ҺpHΪ��������������
�ο��𰸣���1��5?��2��6
��������������ܶȻ�������pH���йؼ��㡣
��1������������ͭ���ܶȻ���������ʽ��֪ ������������Ũ��Ϊ10��5mol/L�����pH����5�� ������������Ũ��Ϊ10��5mol/L�����pH����5��
��2��Cu2��Ũ�Ƚ���ԭ����ǧ��֮һ��ͭ���ӵ�Ũ�ȱ�Ϊ2��10��4mol/L�����Ը���������ͭ����
�Ȼ���������ʽ��֪
����������Ũ��Ϊ10��6mol/L�����pH����6��
�����Ѷȣ���
4������� ��13�֣�������Ԫ��X��Y��Z��Ԫ�����ڱ��е����λ������ͼ��ʾ��
25�棬0��1 mol��L��1M��Һ��MΪY������������ˮ�����pHΪ13��
��1��Y�����ӽṹʾ��ͼΪ ��
��2��X��Z����̬�⻯���ȶ��Խ�ǿ���� ���ѧʽ����
��3�������ô�ĥ�ڲ��������Լ�ƿʢװM��Һ��ԭ���� �������ӷ���ʽ��ʾ����
��4����ҵ�ϣ���X������ȡZ���ʵĻ�ѧ����ʽΪ ��
��5��X�������������ijһԪ�л���ļ��Σ���ѧʽΪKA��A��Ϊ�������Һ��Ӧ�Ļ�ѧ����ʽΪ ������֪25�棬X������������ˮ����ĵ��볣��ΪKal =4��2��10��7��Ka2=5��6��10��11��HA�ĵ��볣��Ka=1��1��10��10��
��̼�͵��Ļ���������������������������ء���̼���ú�������Դ��������Դ��ú�����г����о���ͬ�¶��µ�ƽ�ⳣ����Ͷ�ϱȼ���ֵ�����⡣
��֪��CO(g) + H2O(g) H2(g) + CO2(g)��ƽ�ⳣ�����¶ȵı仯���±��� H2(g) + CO2(g)��ƽ�ⳣ�����¶ȵı仯���±���
��ش��������⣺
��6����������Ӧ������ ��Ӧ������ȡ������ȡ�����
��7��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K= ��
��8��830Kʱ������ʼʱ��C(CO)=2mol/L��C(H2O)=3mol/L��ƽ��ʱCO��ת����Ϊ60%��ˮ������ת����Ϊ ��KֵΪ ��
��9����һ���¡������ܱ������з�����Ӧ��Ni (s)��4CO(g)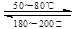 Ni(CO)4(g)����H��0�� Ni(CO)4(g)����H��0��
���ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99.9%�ĸߴ���������˵����ȷ���� ������ĸ��ţ���
A������Ni���������CO��ת���ʣ�Ni��ת���ʽ���
B����С�����ݻ���ƽ�����ƣ���H��С
C����Ӧ�ﵽƽ�����CO�ٴδﵽƽ��ʱ�� CO�������������
D����4v��[Ni(CO)4]= v��(CO)ʱ�������л�������ܶȲ���ʱ,����˵����Ӧ�Ѵﻯѧƽ��״̬
�ο��𰸣�
I����1�� �� ��
��2��CH4
��3��SiO2+2OH-=SiO32-+H2O
��4��SiO2+C Si+CO�� Si+CO��
��5��KA+CO2+H2O=HA+KHCO3
II����6������
��7��K=c(H2)c(CO2)/c(CO)c(H2O)
��8��40%��1
��9��C
���������I��25�棬0��1 mol��L��1M��Һ��MΪY������������ˮ�����pHΪ13��˵��M��ǿ�����X��Y��Z��Ԫ�����ڱ��е�λ���ж�Y��NaԪ�أ���Ӧ������������ˮ�������������ƣ�Ϊǿ���X��CԪ�أ�Z��SiԪ�ء�
��1��Na�����ӽṹʾ��ͼΪ �� ��
��2��C�ķǽ����Դ���Si������C����̬�⻯��CH4���ȶ��Խ�ǿ��
��3����Ϊ���������벣�����еĶ������跴Ӧ����ճ�Խϴ�Ĺ����ƣ����Բ����ô�ĥ�ڲ��������Լ�ƿʢװ����������Һ�����ӷ���ʽ��SiO2+2OH-=SiO32-+H2O;
��4����ҵ���õ���̼��ԭ����������ȡSi���ʣ���ѧ����ʽ��SiO2+C Si+CO��; Si+CO��;
(5)����������ĵ��볣����֪������H2CO3>HA>HCO3-�����Զ�����̼��KA��Һ��Ӧֻ������̼����غ�HA����ѧ����ʽ��KA+CO2+H2O=HA+KHCO3��
II����6���¶����ߣ�ƽ�ⳣ����С��˵�������¶ȣ�ƽ�������ƶ�����÷�Ӧ�Ƿ��ȷ�Ӧ��
��7������ƽ�ⳣ���Ķ��壬�÷�Ӧ��ƽ�ⳣ��K=c(H2)c(CO2)/c(CO)c(H2O)��
��8��830Kʱ������ʼʱ��C(CO)=2mol/L��C(H2O)=3mol/L��ƽ��ʱCO��ת����Ϊ60%����ƽ��ʱc(H2)=c(CO2)=2mol/L��60%=1.2mol/L������ˮ������Ũ��Ҳ��1.2mol/L����ˮ������ת����Ϊ1.2mol/L/3mol/L��100%=40%��ƽ��ʱˮ������Ũ����3mol/L-1.2mol/L=1.8mol/L��CO��Ũ����2mol/L-1.2mol/L=0.8mol/L������K=c(H2)c(CO2)/c(CO)c(H2O)������¶��µ�ƽ�ⳣ����1.22/��0.8��1.8��=1��
��9��A��NiΪ���壬����Ni������ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬����B����С�����ݻ���ѹǿ����ƽ�����ƣ�����H���䣬����C����Ӧ�ﵽƽ�����CO���൱������ѹǿ��ƽ�������ƶ������ٴδﵽƽ��ʱ��CO�����������С����ȷ��D����Ϊ�÷�Ӧ�й���μӣ�����������������仯���ﵽƽ��ʱ������������ٱ仯����������ܶȲ��䣬���Ե������л�������ܶȲ���ʱ,��˵����Ӧ�Ѵﻯѧƽ��״̬����4v��[Ni(CO)4]= v��(CO)��ʾ����Ӧ���ʣ����������淴Ӧ������ȵ������������ж�ƽ��ĵ������ѡC��
���㣺����Ԫ���ƶϣ���ѧ�������д����ѧƽ����ƶ���ƽ�ⳣ����Ӧ��
�����Ѷȣ�����
5��ѡ���� ��5 mL NaCl��Һ�е���һ��AgNO3��Һ,���ְ�ɫ����,�����μ�һ��KI��Һ����,������Ϊ��ɫ,�ٵ���һ��Na2S��Һ����,�����ֱ�ɺ�ɫ,���������仯����,���������ֳ�������ܽ�ȹ�ϵΪ(? )
A��AgCl=AgI=Ag2S
B��AgCl��AgI��Ag2S
C��AgCl��AgI��Ag2S
D��AgI��AgCl��Ag2S
�ο��𰸣�C
���������������AgCl AgI AgI Ag2S,���ܽ��AgCl��AgI��Ag2S�� Ag2S,���ܽ��AgCl��AgI��Ag2S��
�����Ѷȣ���
|  H2(g) + CO2(g)��ƽ�ⳣ�����¶ȵı仯���±���
H2(g) + CO2(g)��ƽ�ⳣ�����¶ȵı仯���±���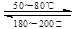 Ni(CO)4(g)����H��0��
Ni(CO)4(g)����H��0��