微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 Fe(OH)3存在如下平衡:Fe(OH)3(s)?Fe3+(aq)+3OH-(aq)常温下其Ksp[Fe(OH)3]=2.6×10-39mol4?L-4
(1)某硫酸铁溶液中[Fe3+]=2.6×10-3mol?L-1,如果生成氢氧化铁沉淀,应调整溶液pH使之大于______.
(2)要使1.3×10-3mol?L-1的硫酸铁溶液中[Fe3+]浓度降至原来的千分之一,若向溶液中加入氢氧化钠溶液,至少将溶液的pH调整为多少?(写出计算过程)
参考答案:(1)Ksp[Fe(OH)3]=2.6×10-39mol4?L-4,c(Fe3+)=2.6×10-3mol?L-1;在常温下如果要生成Fe(OH)3沉淀,则c(Fe3+)×c3(OH-)>2.6×10-39mol4?L-4,所以c(OH-)>32.6×10-39mol4?L-?4?2.6×10-3mol?L-1
本题解析:
本题难度:一般
2、计算题 摩尔盐[xFeSO4・y(NH4)2SO4・zH2O]是一种重要化工原料。其组成可通过下列实验测定:
①称取1.5680 g样品,准确配成100 mL溶液A。
②量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660 g。
③再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol・L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1. 0×10-5mol・L-1,应保持溶液中c(Ba2+)
≥?mol・L-1。
(2)③中发生反应的离子方程式为?,滴定终点的现象是?。
(3)通过计算确定样品的组成(必须写出计算过程)。
参考答案:
(1)1.1×10-5?(2分)
(2)MnO4-+5 Fe2++8H+=Mn2++5 Fe3++4H2O(2分)?
溶液由无色变为浅紫色(紫色、紫红色),且半分钟不褪色 (1分)
(3)n(SO42-)= n(BaSO4)=0. 466g/233g・mol-1=2. 00×10-3 mol (或2.00mmol)?(2分)
n(Fe2+)=5×0. 02000 mol・L-1×10. 00 mL/1000 mL・L-1=1. 000×10-3mol?(1分)
n(NH4+)=2×2. 00×10-3 mol-2×1. 000×10-3mol=2. 000×10-3mol?(1分)
n(H2O)=(1.5680 g×25.00 mL/100.00mL-1.000×10-3mol
×152g・mol-1-1.000×10-3mol×132g・mol-1)/18 g・mol-1
=6. 000×10-3mol?(2分)
x∶y∶z=n(FeSO4)∶n[ (NH4)2SO4]∶n(H2O)=1∶1∶6
该摩尔盐的化学式为FeSO4・(NH4)2SO4・6H2O?(1分)
本题解析:本题是测定物质组成的计算题。
(1)Ksp= c(Ba2+) × c(SO42-)=1.1×10-10?c(Ba2+)= 1.1×10-5 mol・L-1
(3)在步骤②中得到的白色固体为BaSO4,由此计算出SO42-的含量;在步骤③中根据反应方程式计算出溶液中含有的Fe2+的含量,再根据电荷守恒计算出溶液中含有NH4+的含量。但要注意所取的溶液只是原溶液的1/5,计算原溶液中SO42-和Fe2+的物质的量。最后根据总质量计算水的含量,确定组成。
本题难度:一般
3、选择题 下列说法正确的是(? )
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大
B.在一定温度下AgCl的水溶液中,Ag+和Cl-物质的量浓度的乘积是一个常数
C.25oC时Ksp(AgCl)=l.8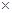 10-10,Ksp(AgI)=1.0×10-16,因此AgCl可以转化为AgI
10-10,Ksp(AgI)=1.0×10-16,因此AgCl可以转化为AgI
D.温度一定时,当溶液中Ag+和Cl-物质的量浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
参考答案:CD
本题解析:溶度积常数只与温度有关系,A不正确;B不正确,因为该溶液不一定是饱和溶液;根据沉淀容易向溶解度更小的方向进行转化可知,C正确;根据Qc和Ksp的关系可知,D也是正确的,答案选CD。
点评:该题是中等难度的试题,也高考中的常见题型,属于中等难度的试题。该题基础性强,注重考查知识的灵活性,侧重考查学生分析问题、解决问题的能力。
本题难度:一般
4、选择题 已知一定量Ca(OH)2固体溶于水后,存在以下平衡状态:Ca(OH)2(s)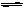 Ca2+(aq)+2OH-(aq),Ksp=4.7×10-6 mol3/L3,下列措施可使Ksp增大的是(?)
Ca2+(aq)+2OH-(aq),Ksp=4.7×10-6 mol3/L3,下列措施可使Ksp增大的是(?)
A.升高温度
B.降低温度
C.加入适量CaO固体
D.加入适量Na2CO3固体
参考答案:B
本题解析:由于Ksp只与难溶电解质的性质和温度有关。而大多数电解质的Ksp随温度的升高而增大,但个别物质如Ca(OH)2,Ksp随温度的升高而降低。
本题难度:一般
5、选择题 已知常温下,AgCl的溶解度大于AgBr的溶解度,将AgCl、AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液发生反应。下列叙述正确的是
A.只有AgBr沉淀生成
B.AgCl沉淀多于AgBr沉淀
C.AgCl沉淀少于AgBr沉淀
D.AgCl、AgBr沉淀等量生成