��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��A��B��C��D��E����Ԫ�أ�AԪ���γɵ�-2�������ӱȺ��ĺ����������8����BԪ�ص�һ��������Ϊ����ɫ���壬�ù�����������������A�ĵ��ʣ�CΪԭ�Ӻ�����12�����ӵĶ��۽�������2.4g?C���������ᷴӦʱ�����ɱ�״���µ�H2?2.24L��D��ԭ��M������7�����ӣ�E��Aͬ�����������ȴ�����3�����ӣ�
��1��C���ӵĽṹʾ��ͼ______��
��2��A��E�⻯����ȶ��ԱȽ�______�����ѧʽ��
��3��A��B��C��D�������Ӱ뾶�ɴ�С˳��______�������ӷ��ű�ʾ��
��4��д��Cu��E������������Ӧˮ����ϡ��Һ��Ӧ�����ӷ�Ӧ����ʽ��______��
��5����һ�ֺ���AԪ�ص���18�����ӵĻ������ϡ����Ļ�����м���ͭƬ����Һ��Ϊ��ɫ��д���÷�Ӧ�����ӷ�Ӧ����ʽ______��
��6��д��ʵ������E���⻯��Ļ�ѧ��Ӧ����ʽ______��
�ο��𰸣�����AԪ���γɵ�-2�������ӱȺ��ĺ����������8������A��������Ϊ8����AΪ��Ԫ�أ�BԪ�ص�һ��������Ϊ����ɫ���壬�ù�����������������A�ĵ��ʣ���BΪ��Ԫ�أ���2.4g?C���������ᷴӦʱ�����ɱ�״���µ�H22.24L��n��H2��=0.1mol��M��C��=2.4g0.1mol=24g/mol����C��������Ϊ24��CΪԭ�Ӻ�����12�����ӵĶ��۽�������C��������Ϊ12����CΪþԪ�أ�D��ԭ��M������7�����ӣ���DΪ��Ԫ�أ�E��Aͬ�����������ȴ�����3�����ӣ�EΪ�ڶ�����Ԫ�أ���������Ϊ5����EΪ��Ԫ�أ�
��1��CΪþ����ʧȥ�������ӣ���þ������2�����Ӳ㣬�����ӵĽṹʾ��ͼ
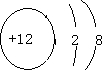
���ʴ�Ϊ��
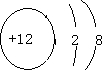
��
��2��AΪ����EΪ���������ǵ��⻯��ֱ�ΪH2O��NH3���ǽ�����O��N�����⻯����ȶ���H2O��NH3���ʴ�Ϊ��H2O��NH3��
��3��A��B��C��D�������ӷֱ�ΪO2-��Na+��Mg2+��Cl-��ֻ��Cl-���������Ӳ㣬�����Ӱ뾶���O2-��Na+��Mg2+�������Ӿ�����ͬ�ĵ��Ӳ��Ų���
��ԭ������Խ������Ӱ뾶ԽС�������Ӱ뾶ΪO2-��Na+��Mg2+���������Ӱ뾶�ɴ�С˳��ΪCl-��O2-��Na+��Mg2+���ʴ�Ϊ��Cl-��O2-��Na+��Mg2+��
��4��E������������Ӧˮ����Ϊ���ᣬCu��ϡ���ᷴӦ��������ͭ��NO��H2O���÷�ӦΪ3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O�����ӷ�ӦΪ
3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O��
��5��AԪ�ص���18�����ӵĻ�����ΪH2O2��Cu��������������������·���������ԭ��Ӧ�����ӷ�ӦΪCu+H2O2+2H+�TCu2++2H2O��
�ʴ�Ϊ��Cu+H2O2+2H+�TCu2++2H2O��
��5��E���⻯��ΪNH3��ʵ�������Ȼ�����������Ʒ�Ӧ���ɰ������÷�ӦΪ2NH4Cl+Ca��OH��2?��?.?CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2?��?.?CaCl2+2NH3��+2H2O��
���������
�����Ѷȣ�һ��
2��ѡ���� ����A�Ļ�ѧʽΪNH5����������ԭ�ӵ�����㶼������Ӧϡ������ԭ�ӵ�������Ӳ�ṹ���������й�˵���У�����ȷ���ǣ�������
A��NH5�м������Ӽ����й��ۼ�
B��NH5���ۡ��е����NH3
C��NH5����Ͷ������ˮ�У��ɲ�����������
D��0.1?mol?NH5���5?mol?N-H��
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� ���л�ѧ�����������ȷ����
[? ]
A��Cl-�Ľṹʾ��ͼ��
B��NH4Cl�ĵ���ʽ��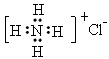
C����ϩ��ʵ��ʽ�����ʽ����CH2
D��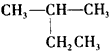 �����ƣ�2-�һ�����
�����ƣ�2-�һ�����
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ���������У��Ⱥ����Ӽ��ֺ����ۼ����ǣ�������
A��NaCl
B��CO2
C��NaOH
D��N2
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ���й�ʯ�������������������Ǵ�ѧ���о���Ա��������������ǿ���ᣬ����ǿ��Ļ�ѧʽ��
CB11H6Cl6���ṹʽ��ͼ��ʾ����11����ԭ�Ӻ�1��̼ԭ�����г�20���塣��ǿ����ԭ�Ӽ�Ļ�ѧ��������
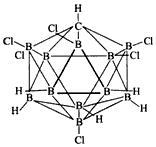
[? ]
A��ֻ�й��ۼ�
B��ֻ�����Ӽ�
C���������Ӽ����й��ۼ�
D����һ�ֽ��ڹ��ۼ������Ӽ�֮���һ�ּ�
�ο��𰸣�A
���������
�����Ѷȣ���