微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 2011年3月11日日本大地震造成日本福岛核电站出现严重事故,由核反应堆泄漏出的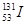 和
和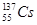 引起全世界的关注,其中
引起全世界的关注,其中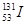 原子核内的中子数为
原子核内的中子数为
A. 53
B. 78
C. 131
D.184
参考答案:B
本题解析:具体的原子表示为A Z X,其中A为质量数,Z为质子数,N(中子数)=A―Z;所以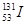 原子核内的中子数=131―53=78
原子核内的中子数=131―53=78
本题难度:简单
2、填空题 (11分)A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子分别位于IA ,? IIIA , VIA族且同周期,B对应碱呈两性,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A ??,B?,C?,D?,E?
(2)写A与E两元素可形成化合物的电子式:??。
(3)写出A、B两元素的最高价氧化物的水化物之间的相互反应的化学方程式:
??。
(4) 比较C、D的最高价氧化物的水化物的酸性的强弱:??。(用化学式表示)
参考答案:(11分)
(1)A:Na,? B:Al,? C:Si,? D:P,? E:S?(每空1分,共5分)
 (2)
(2)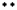




 Na? +? S? +? Na? Na S Na
Na? +? S? +? Na? Na S Na
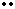 (2分)
(2分)
(3)Al(OH)3+ NaOH ="==" NaAlO2+2H2O?(2分)
(4)H3PO4>H2SiO3?(2分)
本题解析:(1).首先题目给出是短周期元素,因此定位在前三周期中,B原子位于IIIA族且对应碱呈两性,由此推出B是A(第三周期IIIA族)l;A、B、E在同一周期,且A是IA族,E是VIA,由此推出A是Na,E是S。A、B、E最高价氧化物的水化物分别是NaOH、Al(OH)3和H2SO4;C元素的原子序数比B大且最外层电子数比次外层电子数少4,则推出C是Si,D就是P。
(2)Na原子最外电子层上只有1个电子,S原子最外电子层上有6个电子,形成的化合物是Na2S。
(3)A、B最高价氧化物的水化物分别是NaOH、Al(OH)3他们间的反应式为Al(OH)3+ NaOH ="==" NaAlO2+2H2O
(4)Si、P是同一周期的元素,非金属性逐渐减弱,对应的最高价氧化物的水化物的酸性也逐渐减弱。所以H3PO4>H2SiO3
本题难度:一般
3、填空题 回答以下关于第三周期元素及其化合物的问题。
(1)下列能用于判断氧和氟非金属性强弱的是?(选填编号)。
A.气态氢化物的稳定性? B.最高价氧化物对应水化物的酸性
C.单质与氢气反应的难易? D.单质与同浓度酸发生反应的快慢
(2)Be和Al具有相似的化学性质,写出BeCl2水解反应的化学方程式?
(3)常温下,不能与铝单质发生反应的是_________(填序号)
A.CuSO4溶液?B.Fe2O3 ?C.浓硫酸?D.NaOH?E.Na2CO3固体
(4)相同压强下,部分元素氟化物的熔点见下表:
氟化物
| NaF
| MgF2
| SiF4
|
熔点/℃
| 1266
| 1534
| 183
|
?
试解释上表中氟化物熔点差异的原因:?。SiF4分子的空间构型为?,SiF4中Si―F键间的键角?。(选填“相等”、“不相等”或“无法判断”)
(5)Cl2合成有机物时会产生副产物HC1。4HCl+O2 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。
该反应平衡常数的表达式K=?;若反应容器的容积为2L,8min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为? mol/L? min。
参考答案:(1)AC
(2)BeCl2+2H2O  ?Be(OH)2+2HCl
?Be(OH)2+2HCl
(3)B、E
(4)NaF与 MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高。(2分)?
正四面体(1分),相等(1分)
(5)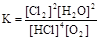 (1分)? 0.0625mol/L? min (1分)
(1分)? 0.0625mol/L? min (1分)
本题解析:(1)判断氧和氟非金属性强弱可依据气态氢化物的稳定性,由于氟没有最高价氧化物对应水化物,故不能通过酸性比较,还可通过单质与氢气反应的难易判断,非金属单质一般不会与酸发生反应,故不可。选AC。
(2)BeCl2是一种强酸弱碱盐,其水解反应的化学方程式BeCl2+2H2O  ?Be(OH)2+2HCl 。
?Be(OH)2+2HCl 。
(3)A.铝单质与CuSO4溶液发生置换反应。B.Fe2O3 不能发生。 C.浓硫酸发生钝化。 D.NaOH与铝生成偏铝酸钠和氢气。 E.Na2CO3固体与铝不发生反应。故常温下,不能与发生反应的是B、E。
(4)NaF与 MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小,Mg2+带2个单位正电荷数比Na+多,故MgF2的熔点比NaF高。SiF4发生SP3杂货,分子的空间构型为正四面体,SiF4中Si―F键间的键角相等。
(5)反应4HCl+O2  ?2Cl2+2H2O,的平衡常数的表达式
?2Cl2+2H2O,的平衡常数的表达式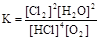 ;则HCl的平均反应速率为(2.5mol-2.25mol)/(2L*8min)= 0.0625mol/L? min。
;则HCl的平均反应速率为(2.5mol-2.25mol)/(2L*8min)= 0.0625mol/L? min。
本题难度:一般
4、选择题 下列关于卤族元素由上到下性质递变规律的叙述,正确的是( )。
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强 ④单质的沸点升高 ⑤阴离子的还原性增强
A.①②③
B.②③④
C.②④⑤
D.①③⑤
参考答案:C
本题解析:F2、Cl2、Br2、I2氧化性依次减弱,其对应的阴离子F-、Cl-、Br-、I-的还原性依次增强,故①叙述错误,⑤叙述正确;F2、Cl2、Br2、I2的颜色由浅黄绿色→黄绿色→深红棕色→紫黑色逐渐加深,②叙述正确;HF、HCl、HBr、HI的稳定性逐渐减弱,③叙述错误;F2、Cl2、Br2、I2在通常情况下其状态变化为气→液→固,则沸点逐渐升高,④叙述正确,故答案为C。
本题难度:一般
5、选择题 下列粒子(或化学键)的数目之比不是1∶1的是
A.氘原子中的质子和中子
B.Na2O2固体中的阴离子和阳离子
C.CO2分子中的σ键和π键
D.常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH-
参考答案:B
本题解析:A.氘原子中的质子和中子都是1个,因此个数比为1:1;错误。B.在Na2O2固体中的阴离子O22-和阳离子Na+个数比为1:2。正确。C.CO2分子结构式是O=C=O,可见在CO2分子中有2个的σ键和2个π键,化学键的数目之比是1∶1。错误。D.在室温下,水的离子积常数是c(H+)・c(OH-)=1×10-14;由于pH=7,所以c(H+)=c(OH-)。因为在同一溶液中,所以物质的量的比等于二者的浓度比,故混合溶液中的H+与OH-的个数比为1:1。错误。
本题难度:简单