|
�߿���ѧ���⡶���ʵķ��롢�ᴿ����Ƶ����Ԥ�⣨2017�����°棩(��)
2017-08-26 01:03:00
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (ÿ��3�ֹ���10�֣����Ṥҵ�з�����Ϊ����������ɷ�ΪSiO2��Fe2O3��Al2O3��MgO��ij̽����ѧϰС���ͬѧ������·����������������н���Ԫ�ص���ȡʵ�顣
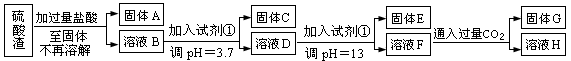
��֪��ҺpH=3.7ʱ��Fe3+�Ѿ�������ȫ��һˮ�ϰ����볣��Kb=1.8��10��5���䱥����Һ��c(OH��)ԼΪ1��10-3mol��L-1����ش�
��1��д��A������������Һ��Ӧ�Ļ�ѧ����ʽ������������������������������������
��2����������������ʹ���Լ��٣��Ʋ��Լ���Ӧ������������������������������������������ĸ��ţ�
A����������
B��������
C����ˮ
D��ˮ
| ��3����ҺD������E��������Ҫ������ҺpH=13�����pH��С�����ܵ��µĺ����������������������дһ�㣩
��4��H�����ʵĻ�ѧʽ����������������������������
��5��������ҺF��c(Mg2+)��������������������25��ʱ��������þ��Ksp=5.6��10-12��
�ο��𰸣���1��SiO2+2NaOH=Na2SiO3+H2O?��2��A
��3��þ���ӳ�������ȫ�����������ܽⲻ��ȫ��?��4��NaHCO3?��5��5.6�� 10�C10 mol/L
�����������1����������ֻ�ж�������������Ӧ������A�Ƕ������裬������������Һ��Ӧ�ķ���ʽ��SiO2+2NaOH=Na2SiO3+H2O��
��2���Լ��ٵ��������к���Һ�е������ӣ���������������������ڰ�ˮ��pH���ֻ����11������Ӧ��ѡ���������ƣ���ѡA��
��3����������ͼ��֪������C������������E��������þ����������������Ʋ��㣬��þ���ӳ�������ȫ�������������ܽ�Ҳ����ȫ��
��4����ҺF���������ƺ�ƫ�����ƵĻ�������ͨ��������CO2�����ɳ�����������������Һ�е���������̼�����ơ�
��5����Һ��OH��Ũ����0.1mol/L�����Ը����ܶȻ�������֪����Һ��c(Mg2+)��5.6��10-12��0.12��5.6�� 10�C10 mol/L��
�����Ѷȣ�һ��
2��ѡ���� ���ữ����ʵ���о������õķ���������˵����ȷ����
A����߸�����ص�������������Ũ�����ữ
B������Fe2����ˮ�⣬��ϡ�����ữ
C������ij±�������Ƿ���Ԫ�أ��ȼ�HNO3�ữ���ټ�AgNO3��Һ����
D��ȷ����Һ�к���SO42��ʱ�����������ữ���ټ�BaCl2��Һ����
�ο��𰸣�D
���������A�������ܱ��������������Ӧ�������ữ������B��ϡ�������ǿ�����ԣ�������Fe2��������C��±�����е�±ԭ�����ڼ���������ˮ�⣬����±�����ӣ������ܣ�����D�����ų�̼������ӡ�����������ӡ������Ӹ��ţ���ȷ��
�����Ѷȣ�һ��
3��ѡ���� ������Һ�У����ʵ����ʵ���Ũ��Ϊ1mol?L-1?����
A.��40?g?NaOH����1?L?ˮ���õ���Һ
B.��5?mol?L-1��H2SO4��Һ100mlϡ�ͳ�500ml
C.NA���Ȼ����������ˮ���1L��Һ
D.c��K+��Ϊ1?mol?L-1��K2SO4��Һ
�ο��𰸣�BC
���������������A��40gNaOH�����ʵ���Ϊ1mol������ˮ���1L��ҺŨ��Ϊ1mol?L-1��
B������n=cv���⣻
C��NA���Ȼ���������ʵ�����1mol��
D����������صĻ�ѧʽ��֪������Ũ��Ϊ�����Ũ�ȵ�2����
���A��40gNaOH�����ʵ���Ϊ1mol������ˮ���1L��ҺŨ��Ϊ1mol?L-1�������ܼ������Ϊ1L����A����
B������n=cv=5?mol?L-1��0.1L=0.5mol����Һ�������0.5L��������ҺŨ��Ϊ1mol/L����B��ȷ��
C��NA���Ȼ���������ʵ�����1mol������ˮ���1L��ҺŨ��Ϊ1mol/L����C��ȷ��
D��������Ũ��Ϊ�����Ũ�ȵ�2������K+Ϊ1mol?L-1��K2SO4��ҺŨ��Ϊ0.5mol/L����D����
��ѡBC��
���������⿼�����ʵ���Ũ�ȵ���������㣬�ѶȽ�С��ע�����ʵ���Ũ�������ָ��Һ�������������ˮ���ʱ仯�������
�����Ѷȣ�һ��
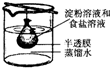
4��ѡ���� ��10mL���۽����5mL�Ȼ�����Һ��Ϻ����ð�Ĥ�ƳɵĴ��ڣ����˴���������ˮ�У���ͼ��ʾ����2min��ֱ�ȡ���ں��ձ���Һ�����ʵ�飮����˵����ȷ���ǣ�������
A������Һ�������������Һ���ޱ仯
B���ձ���Һ������ˮ�����ɫ
C������Һ������ˮ����
D���ձ���Һ�������������Һ���а�ɫ��������
|