|
高考化学必考知识点《化学反应速率》高频考点巩固(2017年模拟版)(十)
2017-08-26 01:08:53
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 一密封体系中发生下列反应:N2 +3H2 2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图: 2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图:

回答下列问题:
(1)处于平衡状态的时间段是______.
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化?
、 、
(3)下列各时间段时,氨的百分含量最高的是______.
A.t0~t1
B.t2~t3
C.t3~t4
D.t5~t6
|
参考答案:(1)t0~t1、t2~t4、t5~t6(2)升高温度,加了催化剂,降低压强(3)t0~t1
本题解析:本题是考查反应速率与化学平衡内在联系的一道好题.处于平衡状态时,正逆反应速率必定相等,从图(1)可看出t0~t1、t2~t4、t5~t6时间段时反应处于平衡状态.
t1时刻,条件变化使V正、V逆都加快,且V逆>V正,平衡向逆反应方向移动,对照反应式可看出条件变化应是“升高温度”.t3时刻,V正、V逆都同幅度加快,应是“加了催化剂”.t4时刻时,V正、V逆都减慢,且V正<V逆,平衡逆移,所以是由“降低压强”引起的.
由于t1~t2时间段和t4~t5时中,平衡都向逆反应方向移动,氨百分含量都减小,所以应是t0~t1时间段中氨百分含量最高。
考点:化学平衡
本题难度:一般
2、选择题 温度为500℃时,反应4NH3+5O2 4NO+6H2O在2L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为(?) 4NO+6H2O在2L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v (x)为(?)
A.v(O2)=0.01mol/(L?s)
B.v(NO)=0.01mol/(L?s)
C.v(H2O)=0.006mol/(L?s)
D.v(NH3)=0.005mol/(L?s)
参考答案:D
本题解析:NO反应速率为0.3mol/2L?0.5min = 0.3mol/(L?min)= 0.005mol/(L?s),反应速率之比等于化学计量数之比。故选择D
本题难度:一般
3、填空题 密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5
n(NO)(mol)
0.020
0.010
0.008
0.007
0.007
0.007
|
(1)写出该反应的平衡常数表达式:K=______.已知:K(300℃)>K(350℃),该反应是______热反应;
(2)图中表示NO2的变化的曲线是______.用O2表示从0~2s内该反应的平均速率v=______;
(3)能说明该反应已经达到平衡状态的是______;
a、v(NO2)=2v(O2)?b、容器内压强保持不变
c、v逆(NO)=2v正(O2)?d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是______.
a、及时分离出NO2气体?b、适当升高温度
c、增大O2的浓度?d、选择高效的催化剂.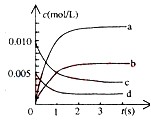
参考答案:(1)化学平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,本反应中K=c(NO2)c2(?NO)c(O2),升高温度平衡常数减小,说明升高温度平衡向逆反应方向移动,则正反应放热,故答案为:K=c(NO2)c2(?NO)c(O2);放热;
(2)由图象可知c为NO的变化曲线,d为氧气的变化曲线,根据方程式可知NO和NO2的反应速率相等,则b为NO2的变化曲线,
0~2s内v(O2)=0.005mol/L-0.002mol/L2s=1.5×10-3mol/(L?s),
故答案为:b;?1.5×10-3mol/(L?s);
(3)a、反应无论是否达到平衡状态,都满足速率之比等于化学计量数之比,故a错误;
b、反应前后气体的化学计量数之和不相等,则达到平衡状态时,压强不变,故b正确;
c、v逆(NO)=2v正(O2)说明达到平衡状态,故c正确;
d、容器的体积不变,反应物和生成物都是气体,则无论是否达到平衡状态,密度都不变,故d错误.
故答案为:b、c.
(4)a、及时分离出NO2气体,平衡向正反应方向移动,但反应的速率减小,故a错误;
b、升高温度平衡向逆反应方向移动,故b错误;
c、增大O2的浓度,反应速率增大,平衡向正反应方向移动,故c正确;
d、加入催化剂平衡不移动,故d错误.
故答案为:c.
本题解析:
本题难度:一般
4、选择题 增大压强对下列反应的速率无影响的是( )
A.CO2(g)+Ca(OH)2(aq)=CaCO3(s)↓+H2O(l)
B.H2(g)+I2(g)

2HI(g)
C.NaCl(aq)+AgNO3(aq)=AgCl(s)↓+NaNO3(aq)
D.N2(g)+3H2(g)

2NH3(g)
参考答案:A、二氧化碳是气体,对于有气体参加的反应,增大压强可增大反应速率,故A不符合;
B、对于反应H2(g)+I2(g)

2HI(g),反应混合物都是气体,增大压强可增大反应速率,故B不符合;
C、反应没有气体参加,压强对液体、固体的体积影响忽略不计,增大压强对反应的速率基本无影响,故C符合;
D、对于反应N2(g)+3H2(g)

2NH3(g),反应混合物都是气体,增大压强可增大反应速率,故D不符合.
故选C.
本题解析:
本题难度:一般
5、选择题 在四种不同条件下,反应A + B = 2C + 2D的反应速率如下,其中最快的是( )
A.V(A) =0.15 mol・L-1・S-1 B.V(B) =0.3 mol・L-1・S-1
C.V(C) =0.4 mol・L-1・S-1 D.V(D) =0.45 mol・L-1・S-1
参考答案:B
本题解析:A.v(A)=0.15 mol?L-1?s-1;
B.v(A)=v(B)=0.3 mol?L-1?s-1;
C.v(A)=1/2v(C)=0.2 mol?L-1?s-1;
D.v(A)=1/2v(D)=0.225 mol?L-1?s-1,
则反应速率最大的为B.
考点:化学反应速率
本题难度:一般
| 