微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某学习小组,用稀HNO3与大理石反应过程中质量减小的方法,探究影响反应速率的因素。所用HNO3浓度为1.00 mol・L-1、2.00 mol・L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.00 mL、大理石用量为10.00 g。
实验设计如表:
编号
| T/K
| 大理石规格
| HNO3浓度
|
①
| 298
| 粗颗粒
| 2.00 mol・L-1
|
②
| 298
| 粗颗粒
| 1.00 mol・L-1
|
③
| 308
| 粗颗粒
| 2.00 mol・L-1
|
④
| 298
| 细颗粒
| 2.00 mol・L-1
|
将相应的实验目的填入下列空格中:
(1)实验①和②探究 对该反应速率的影响;
(2)实验①和③探究 对该反应速率的影响;
(3)实验①和④探究 对该反应速率的影响
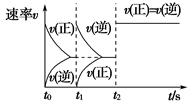
2、选择题 在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
 ?
?
甲 ? 乙
A.图甲,p1>p2,a<3
B.图甲,T1<T2,Q>0
C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体
D.图乙,如果a=3,t2时表示向体系中加入了催化剂或增大压强
3、填空题 催化剂在生产和科技领域中起着重大作用.为比较Fe3+、Cu2+和MnO2对H2O2分解反应的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题.
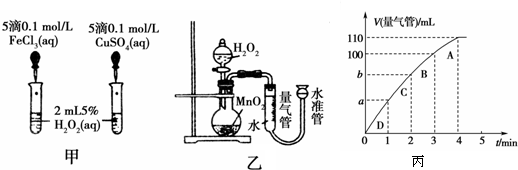
(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论______(填“合理”或“不合理”),理由是______.
(2)同学Y利用乙装置探究MnO2对H2O2分解的催化效果.将50mL?H2O2一次性加入盛有0.10mol?MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)/mL]和时间(t/min)的关系如丙图所示.
①b______(填“<”、“>”或“=”)90mL,原因是______.
②同学Y除了探究MnO2对H2O2分解速率的影响情况,还可得出______对H2O2分解速率的影响情况.
(3)催化剂能加快反应速率,是因为它能改变反应的路径,使发生反应所需的活化能______(填“升高”“降低”“不变”).
4、简答题 在2七℃时,向100mL含氯化氢19.6g的盐酸溶液里放入七.60g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2min末,收集到1.12L(标准状况)氢气.在此之后,又经过9min,铁粉完全溶解.则
(1)在前2min?内用FeCl2表示的平均反应速率是______mol?L-1?min-1.
(2)在后9min内用HCl表示的平均反应速率是______mol?L-1?min-1.
5、填空题 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
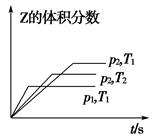
(1)根据下表中数据,在下图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线
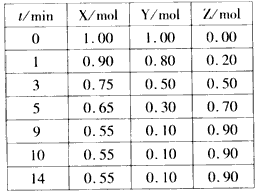
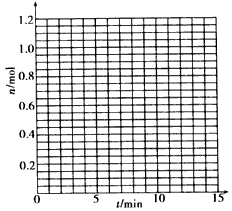
(2)体系中发生反应的化学方程式是_____________;
(3)列式计算该反应在0-3 min时间内产物Z的平均反应速率:_____________,
(4)该反应达到平衡时反应物X的转化率α等于_____________;
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:
1_____________,2_____________,3_____________。