��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ȼ�ϵ���ǽ�������ֱ�ͨ���أ���������20%��40%��KOH��Һ�Ķ��̼�缫����缫��ӦΪ��2H2 +4OH- - 2e-=4H2O��O2 +2H2O+ 2e-=4OH-��������������ȷ����
[? ]
A��ͨ��H2��һ����������ͨ��O2��һ���Ǹ���
B��ͨ��O2��һ����������ͨ��H2��һ���Ǹ���
C����ع���һ��ʱ��������Һ��pH����
D������ڹ���ʱ��������������pH����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2������� (6��) ��A��B��C��D���ֽ������±���װ�ý���ʵ�飬����ʵ������ش�٢ڢ�
�ο��𰸣���6�֣�?2H+ +2e--==?H2����C��B��D��A��B��C
�������������A�����ܽ⣬˵��A�Ǹ�����ʧȥ���ӣ�����������Ӧ����A�Ľ�����ǿ��B�ġ����������������ӷŵ������������缫��Ӧʽ��2H+ +2e--==?H2����C���������ӣ���˵��C����������Һ�е�ͭ���ӷŵ磬����ͭ���γɣ������������C��B������B�Ľ�����ǿ��C�ģ�A��D����ԭ���ʱ��A�������������˵��A����������Һ�е������ӷŵ���������������D�Ľ�����ǿ��A�ġ��������������ֽ����Ľ�����ǿ��˳����D��A��B��C��
��������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ���ݴ˿��Խ����йص��жϡ�
�����Ѷȣ�һ��
3������� ��ͼ�е缫a��b�ֱ�ΪAg�缫��Pt�缫���缫c��d����ʯī�缫��ͨ��һ��ʱ���b�缫��֣�����c��d�缫����������������Ϲ��ռ���336mL����״̬�����壮�ش�
��1��ֱ����Դ�У�MΪ______����
��2��Pt�缫�����ɵ�������______��������Ϊ______g��
��3����Դ����ĵ��ӣ������ʵ�����缫b��c��d�ֱ����ɵ����ʵ����ʵ���֮��Ϊ��2��______��______��______��
��4��AgNO3��Һ��Ũ��______�����������С�����䡱����ͬ����AgNO3��Һ��pH______��H2SO4��Һ��Ũ��______��H2SO4��Һ��pH______��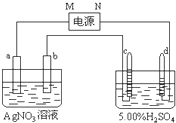
�ο��𰸣���1����������֪���缫a��b��û���������ɣ���a��������bΪ����������M��ԭ����������ʴ�Ϊ������
��2�����ϡ���ᷴӦʱ����ͨ��һ��ʱ���c��d�������ռ���336mL���壨��״����������������2H++2e-�TH2������������4OH--4e-�TO2��+2H2O��ʵ���ϵ�����ˮ����ط�ӦʽΪ��2H2O?���?.?2H2��+O2�������ݷ���ʽ֪���������������ռ�������23���Ի�������������������224mL������2H++2e-�TH2��֪��ת�Ƶ��ӵ����ʵ�����0.02mol������������ת�Ƶ�������ȣ���Ƴ�������������������Ϊ
Ag++e-=Ag
?1mol 108g?
0.02mol?2.16g
�ʴ�Ϊ������2.16g��
��3��b�缫�ϵĵ缫��ӦʽΪ��Ag++e-=Ag
C���缫�ϵĵ缫��ӦʽΪ��4OH--4e-=2H2O+O2��
d���缫�ϵĵ缫��ӦʽΪ��2H++2e-=H2��
����ת�Ƶ��ӵ����ʵ�����2mol����������2mol����������0.5mol����������1mol������
���Ե��ӵ����ʵ�����缫b��c��d�ֱ����ɵ����ʵ����ʵ���֮��Ϊ��2��2��0.5��1��
�ʴ�Ϊ��2��0.5��1��
��4���ڲ��缫�϶���ʱ�������ϵĵ缫��ӦʽΪAg-e-=Ag+�������ϵĵ缫��ӦʽΪAg++e-=Ag��������������Һ��Ũ�Ȳ��䣬��Һ��pH���䣻���ϡ������Һʱ����������2H++2e-�TH2������������4OH--4e-�TO2��+2H2O��ʵ���ϵ�����ˮ����Һ�е����ʲ��䣬�ܼ����٣�����ϡ�����Ũ��������Һ��pHֵ��С��
�ʴ�Ϊ�����䣻���䣻����С��
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼΪͭпԭ���ʾ��ͼ������˵����ȷ����
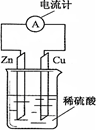
A��������ͭƬͨ����������пƬ
B���ձ�����Һ����ɫ
C��пƬ���ܽ�
D����װ���ܽ�����ת��Ϊ��ѧ��
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã������װ��ͼ��֪��п�Ǹ�����ʧȥ���ӣ�ͭ����������Һ�е��������������õ����ӣ�������ԭ��Ӧ����������ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�������ȷ�Ĵ�ѡC��
�����������Ǹ߿��еij������㣬���ڻ���������Ŀ��顣����Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ���������װ��ͼ������ü��ɣ�����������ѧ����������������
�����Ѷȣ���
5��ʵ���� ��15�֣���������������Ӧ����A��NaOH + HCl =" NaCl" + H2O
��B��2FeCl3 + Cu = 2FeCl2 + CuCl2
��1����������Ӧ���ʣ��ж��ܷ���Ƴ�ԭ���(��ܡ����ܡ�)��A�� ��B�� ��
��2�����(A��B)���ܣ�˵����ԭ�� ��
��3�����(A��B)���ԣ���д�������������ϼ���缫��Ӧʽ���������Һ
������ �� ��
������ �� ��
�������Һ�� ��
�ο��𰸣���1����A�����ܣ�1�֣� ��B���� ��1�֣�
��2��A��Ӧ�Ƿ�������ԭ��Ӧ ��2�֣�
��3��������Cu��2�֣���Cu-2e-=Cu2+��2�֣�
������ʯī��2�֣�������������ɣ���2Fe3++2e-=2Fe2+��3�֣�
�������Һ���Ȼ�����Һ��2�֣�
�����������1�����ڵ��ӵĶ����˶��γɵ���������ֻ��������ԭ��Ӧ������Ƴ�ԭ��أ�A���кͷ�Ӧ����ʾ������ԭ��Ӧ��������Ƴ��е���B��������ԭ��Ӧ�����ԡ�
��3������B���ܷ�Ӧʽ��֪��ͭʧȥ���ӣ�����ԭ����������ԭ��صĸ�������������ֻ�ý���������ͭ���ɡ��Ȼ����õ����� 91ExAm.org����˵������Һ���Ȼ�����
�����Ѷȣ�һ��