|
高考化学知识点总结《原电池原理》高频考点特训(2017年练习版)(六)
2017-08-26 01:09:59
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
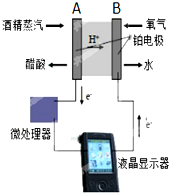
1、选择题 酒后驾车人员体内酒精含量的检测装置如图所示,下列说法不正确的是( )
A.该检测装置实现了将化学能转化为电能,且单位时间内通过电量越大,酒精含量越高
B.电极A的反应:H2O+C2H5OH-4e-=CH3COOH+4H+
C.电极B是正极,且反应后该电极区pH值减小
D.电池反应:O2+C2H5OH=CH3COOH+H2O
|
参考答案:A、该装置是将化学能转变为电能的装置,属于原电池,原电池放电时,单位时间内通过电量越大,需要的燃料越多,则酒精含量越高,故A正确;
B、该原电池中,投放酒精的电极是负极,负极上乙醇失电子和水反应生成乙酸和氢离子,电极反应式为:H2O+C2H5OH-4e-=CH3COOH+4H+,故B正确;
C、原电池投放氧化剂的电极是正极,正极上氧气得电子和氢离子反应生成水,溶液中氢离子浓度减小,pH增大,故C错误;
D、该原电池的反应是乙醇被氧化生成乙酸和水,电池反应式为O2+C2H5OH=CH3COOH+H2O,故D正确.
故选C.
本题解析:
本题难度:一般
2、填空题 火力发电厂释放出大量氮氧化物(NOx)、二氧化硫和二氧化碳等气体而造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g) +CO2(g)+2H2O(g) △H1= -574 kJ/mol
CH4(g)+4NO(g) =2N2(g)+CO2(g)+2H2O(g) △H2= -1 160 kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为______________________
(2)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g)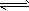 CH3OH(g) +H2O(g) △H3 CH3OH(g) +H2O(g) △H3
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图甲所示,则上述CO2转化为甲醇反应的△H3____(填 “>”“<”或“=”)0。

②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间的变化曲线如图乙所示。下列说法正确的是____(填字母代号)。
A.第10 min后,向该容器中再充入1mol CO2和3 mol H2,则再次达到平衡时c(CH3OH) =1.5 mol/L
B.0~10 min内,氢气的平均反应速率为0.075 mol/(L・min)
C.达到平衡时,氢气的转化率为0. 75
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
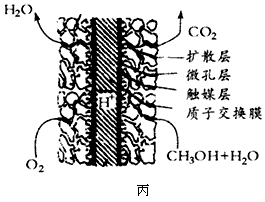
③甲醇燃料电池的结构如图丙所示。其工作时正极的电极反应式可表示为__________________
(3)脱硫。某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。设废气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为___________。
(4)硫酸铵和硝酸铵水溶液的pH<7,其原因可用一个离子方程式表示为:_____________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH =7,则溶液中c(Na+)+c(H+)____(填“>”“=”或 “<”)c(NO3-)+c(OH-)。
参考答案:(1) CH4(g) +2NO2(g) =N2(g) + CO2(g) +2H2O( g) △H = - 867 kJ/mol
(2)①<;②CE;③O2+4e-+4H+=2H2O
(3)12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3
(4)NH4++H2O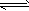 NH3・H2O+H+;< NH3・H2O+H+;<
本题解析:
本题难度:困难
3、实验题 (5分)某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:

参考答案:
本题解析:
本题难度:一般
4、填空题 节约能源、保护资源等已成为实现人类可持续发展的重要课题。
(1)原电池是将化学能转化为____能的装置。人类有待于开发和利用的新能源有 ____(写出一种即可)。在25℃、101 kPa时,1 mol CH4 (g)完全燃烧生成CO2(g)和H2O(l),放出890. 31 kJ的热量,该反应的热化学方程式可表示为 ______________。
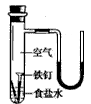
(2)下图是铁的吸氧腐蚀实验。若装置的气密性良好,且开始时U形管两端的红墨水液面相平,则一段时间后,能观察到铁钉生锈,U形管的液面变为____(填“左高右低”或“左低右高”),其正极的电极反应式为____。
(3)下列防止地下钢管锈蚀的措施中,不正确的是____。
A.使它与电源负极相连
B.使它与铜板相连
C.在钢管表面喷油漆
D.使它与锌板相连
参考答案:(1)电 ;太阳能、氢能、核能、风能等; CH4 (g)+2O2(g)==CO2(g)+2H2O(l) △H=-890. 31 kJ/mol
(2)左高右低; 2H2O+O2+4e-==4OH-
(3)B
本题解析:
本题难度:一般
5、填空题 用惰性电极电解下列物质的水溶液,电解过程中,溶液的pH依次为升高、降低、不变的是( )
A.NaCl、CuSO4、Na2SO4
B.HCl、HNO3、CuSO4
C.CaCl2、NaCl、KNO3
D.AgNO3、CaCl2、Ca(NO3)2
参考答案:A、电解NaCl时会生成氢气和氯气单质以及氢氧化钠,电解CuSO4时,生成铜和氧气以及硫酸,电解Na2SO4 生成氢气和氧气,即电解水型的,溶液的PH依次为升高,降低,不变,故A正确;
B、电解HCl生成氯气和氢气,电解本身,电解HNO3时生成氢气和氧气,即电解水型的,电解CuSO4时,生成铜和氧气以及硫酸,溶液的PH依次为升高,降低,降低,故B错误;
C、电解CaCl2时生成氢氧化钙、氯气和氢气,电解NaCl时会生成氢气和氯气单质以及氢氧化钠,电解KNO3时,生成氢气和氧气,即电解水型的,溶液的PH依次为不变,升高,不变,故C错误;
D、电解AgNO3会生成硝酸、银和氧气,电解CaCl2会生成氢气和氯气,电解Ca(NO3)2时会生成氢气和氧气,溶液的PH依次为降低,降低,不变,故D错误.
故选A.
本题解析:
本题难度:一般
| 

