微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
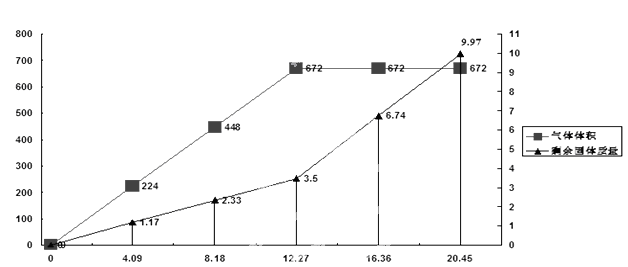
1、实验题 为检验一批因露置而部分变质的Ba(OH) 2药品的成分,某化学探究性学习小组设计了方案对其进行分析:将20.45g药品分成五等分,逐渐加入100mL1 mol/L的盐酸中,并充分搅拌,测得生成气体的体积(已换算为标准状况下)、剩余固体的量与固体加入量的关系如图所示。考虑到某地附近为硫酸工业区,该小组同学判断此药品可能含三或四种成分。
(1) 写出硫酸工业尾气与过量的Ba(OH) 2反应的离子方程式:?
(2)提出以下三种合理假设:(已知在空气中Ba(OH) 2很难生成酸式盐)
假设一:药品成分为Ba(OH) 2和BaSO4、BaSO3;假设二:药品成分为Ba(OH) 2和________________;
假设三:药品成分为Ba(OH) 2和________________。
(3)实验验证:为确定该药品的成分,该小组利用上述实验中生成的气体,选择适当的试剂进行探究,请设计合理方案填入下表:
实验操作
| 预期实验现象和结论
|
?
| 若____________________,假设一成立;
若____________________,假设二成立;
若____________________,假设三成立。
|
?
(4)问题讨论:若经试验验证,此药品为四种成分混合物,该小组同学认为由上述曲线可知,当所加固体质量为12.27 g时,药品成分与盐酸刚好完全反应,你认为该组同学的判断是否正确______。(填“是”或者“否”)
参考答案:(1)Ba2++2OH-+SO2=BaSO3↓+H2O?
(2)假设二: BaSO4、BaCO3?假设三:BaSO4、BaCO3、BaSO3
(3)
实验操作?
预期实验现象和结论
①品红溶液、②足量的酸性高锰酸钾溶液、③澄清石灰水
若_①褪色,②颜色变浅,③无明显现象,假设一成立;
若①和②无明显现象,③变浑浊,假设二成立;
若①褪色,②颜色变浅,③变浑浊,假设三成立。
?
(4)否
本题解析:(1)硫酸工业尾气主要含有SO2,它与过量的Ba(OH) 2反应的离子方程式为Ba2++2OH-+SO2= BaSO3↓+H2O。(2)根据二者发生的反应和已知的假设情况可以确定假设二BaSO4、BaCO3 ;假设三BaSO4、BaCO3、BaSO3。(3)把反应产生的气体①分别通入到品红溶液中,②足量的酸性高锰酸钾溶液、③澄清石灰水。若品红溶液褪色,就证明气体中含有含有SO2,原固体中含有BaSO3;足量的酸性高锰酸钾溶液中,溶液颜色变浅,就证明产生了SO2,原固体中含有BaSO3;澄清石灰水无明显现象,就证明无CO2产生,原固体中没有BaCO3.即证明假设一成立。若①和②无明显现象,③澄清石灰水变浑浊,则证明假设二成立;若①品红溶液褪色,②酸性高锰酸钾溶液颜色变浅,③澄清石灰水变浑浊,则证明假设三成立。(4)由图像可知放出的气体体积最大值是672ml。在加入固体为12.27g时,气体体积为672ml,可能是药品成分与盐酸刚好完全反应,也可能在质量小于12.27g时已经反应完全。放出气体的体积就已经达到最大值。因此该组同学的说法是有偏差的。
本题难度:一般
2、选择题 为了除去KCl中少量的MgSO4和CaCl2杂质,需要进行下列六项操作,其正确操作的先后顺序是……( )
①加水溶解 ②加热蒸发得到晶体 ③加入过量的BaCl2④加入过量的盐酸 ⑤加入过量的碳酸钾 ⑥过滤
A.①③⑤⑥④②
B.①⑤③④⑥②
C.①③④⑥⑤②
D.①④③⑤⑥②
参考答案:A
本题解析:首先把样品溶解于水配成溶液,然后加入过量的BaCl2溶液除去SO42-,由于加过量的BaCl2引入的钡离子,还有原来溶液中含有的Mg2+、Ca2+可加入K2CO3来除去,最后加过量的盐酸除去引入的CO32-离子。
本题难度:一般
3、选择题 下列各组混合物中,能用分液漏斗进行分离的是
[? ]
A.酒精和水
B.碘和四氯化碳
C.水和四氯化碳
D.汽油和植物油
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列各组混合物不能用分液漏斗分离的是( )
A.四氯化碳和碘
B.花生油和水
C.四氯化碳和水
D.水和汽油
参考答案:A
本题解析:
本题难度:一般
5、选择题 为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是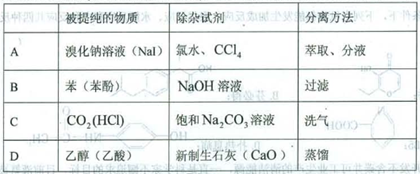
参考答案:D
本题解析:A、氯水具有氧化性,能将溴化钠中的溴离子和碘化钠中的碘离子氧化,不会得到溴化钠,故A错误。B、氢氧化钠与苯酚反应生成苯酚钠,而由于苯不溶于水,应该使用分液的方法分离,错误。C、碳酸钠溶液同样会吸收二氧化碳,所以应该换成饱和碳酸氢钠溶液,错误。D、乙酸与生石灰反应生成乙酸钙,为离子化合物。与乙醇相比,乙醇的沸点低得多,所以D正确。
点评:本题考查物质的分离提纯,题目难度不大,注意根据物质的性质差异性选择物理或化学方法进行分离。
本题难度:一般
|