��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��300mL���ܱ������У��������۲�����һ������CO���壬һ�������·�����Ӧ��Ni��s��+4CO��g��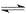 Ni(CO)4��g������֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ�±�������˵����ȷ����
Ni(CO)4��g������֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ�±�������˵����ȷ����
�¶ȡ�
| 25
| 80
| 230
|
ƽ�ⳣ��
| 5��104
| 2
| 1.9��10-5
|
?
A����������Ni(CO)4��g���ķ�ӦΪ���ȷ�Ӧ
B��25��ʱ��ӦNi(CO)4��g��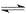 Ni��s��+4CO��g����ƽ�ⳣ��Ϊ0.5
Ni��s��+4CO��g����ƽ�ⳣ��Ϊ0.5
C����80��ʱ�����ijʱ�̣�Ni(CO)4��COŨ�Ⱦ�Ϊ0.5mol/L�����ʱv������>v���棩
D��80��ﵽƽ��ʱ�����n��CO��=0.3mol����Ni(CO)4��ƽ��Ũ��Ϊ2mol/L
�ο��𰸣�D
���������
����֪�����ݿ��Կ����������¶ȣ�ƽ�ⳣ�����٣�˵��ƽ�����淽���ƶ�������Ӧ�Ƿ��ȷ�Ӧ��A����25��ʱ��ӦNi��CO��4��g��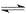 Ni��s��+4CO��g��ʱ����ƽ�ⳣ����1/��5��104����B����80��ʱ��Qc=0.5/0.54>2��˵��ƽ�����淽���ƶ���C����80��ʱ���ٶ�n��CO��=0.3mol����Ni��CO��4��ƽ��Ũ��Ϊ2mol/L������ƽ�ⳣ�������У�2/��0.3/0.3L��4=2�����Լٶ�������D��ȷ����ѡD
Ni��s��+4CO��g��ʱ����ƽ�ⳣ����1/��5��104����B����80��ʱ��Qc=0.5/0.54>2��˵��ƽ�����淽���ƶ���C����80��ʱ���ٶ�n��CO��=0.3mol����Ni��CO��4��ƽ��Ũ��Ϊ2mol/L������ƽ�ⳣ�������У�2/��0.3/0.3L��4=2�����Լٶ�������D��ȷ����ѡD
�����Ѷȣ�һ��
2��ѡ���� ��һ�������£��ϳɰ���Ӧ�ﵽ��ѧƽ����������NH3�����ռ25%����ά�ַ�Ӧ�������䣬��Ӧ����С�������ԭ��Ӧ������ı�ֵΪ��?��
A��1�U5
B��1�U4
C��1�U3
D��1�U2
�ο��𰸣�A
����������跴Ӧ����������ΪV����NH3���Ϊ0.25V��

2? 2
0.25V? x
x=0.25V������Ӧ�������С0.25V��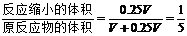 ���𰸣�ѡA��
���𰸣�ѡA��
�����Ѷȣ�һ��
3��ѡ���� ��һ���ܱյ������з������·�Ӧ��2SO2(g)��O2(g) 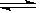 2SO3(g)����Ӧ������ijһʱ��SO2��O2��SO3��Ũ�Ⱦ�Ϊ0.2 mol��L-1�����ﵽƽ��ʱ���ܵ������ǣ�?��
2SO3(g)����Ӧ������ijһʱ��SO2��O2��SO3��Ũ�Ⱦ�Ϊ0.2 mol��L-1�����ﵽƽ��ʱ���ܵ������ǣ�?��
A��c(SO3)="0.4" mol��L-1
B��c(SO3)= c(SO2)="0.15" mol��L-1
C��c(SO2)="0.25" mol��L-1
D��c(O2)="0.3" mol��L-1
�ο��𰸣�C
������������淴Ӧ�ķ�Ӧ�ﲻ����ȫת�������������
A������c(SO3)="0.4" mol��L-1?��Ӧ��Ҫ����ȫת���������B�������ﵽƽ��ʱ������������������Ũ�Ȳ�������ȣ�C��ȷ��D������c(O2)="0.3" mol��L-1������������Ҫ����ȫת��������ӦΪ���淴Ӧ��
�����Ѷȣ���
4��ѡ���� һ�����Ļ���������ܱ������з�����Ӧ��mA��g��+nB��g�� pC��g�����ﵽƽ��ʱ��ά���¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ�µ�ƽ��ʱ������C��Ũ�ȱ�Ϊԭƽ��ʱ��1.9����������˵����ȷ���ǣ�?��
pC��g�����ﵽƽ��ʱ��ά���¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ�µ�ƽ��ʱ������C��Ũ�ȱ�Ϊԭƽ��ʱ��1.9����������˵����ȷ���ǣ�?��
A��m+n��p
B��m+n��p
C��ƽ��������Ӧ�����ƶ�
D��C��������������
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
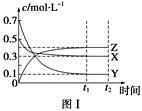
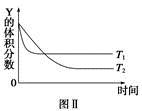
5��ѡ���� ij�¶�ʱ�����ܱ������У�X��Y��Z��������Ũ�ȵı仯��ͼ����ʾ���������������䣬���¶ȷֱ�ΪT1��T2ʱ��Y�����������ʱ���ϵ��ͼ����ʾ�������н�����ȷ����
 ��
��
A���÷�Ӧ���Ȼ�ѧ����ʽΪX(g)��3Y(g)  2Z(g)����H��0
2Z(g)����H��0
B���������������䣬�����¶ȣ������淴Ӧ�ٶȾ�����X��ת���ʼ�С
C���ﵽƽ����������������䣬��С���������ƽ�����淴Ӧ�����ƶ�
D���ﵽƽ����������������䣬ͨ��ϡ�����壬ƽ��������Ӧ�����ƶ�
�ο��𰸣�B
�������������ͼ��ͼ����֪X(g)��3Y(g)  2Z(g)
2Z(g)
��H��0��A����B�ԣ���ѹ��ƽ�����ƣ�C���������º�ѹ��ͨ��ϡ�����壬ƽ�����ƣ������º���ͨ��ϡ�����壬ƽ�ⲻ�ƶ���D����
�����Ѷȣ�һ��