��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ں����ܱ������У���CO�ϳɼ״���CO(g) + 2H2(g)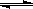 CH3OH(g)���������������������£��о��¶ȶԷ�Ӧ��Ӱ�죬ʵ��������ͼ��ʾ������˵����ȷ����
CH3OH(g)���������������������£��о��¶ȶԷ�Ӧ��Ӱ�죬ʵ��������ͼ��ʾ������˵����ȷ����
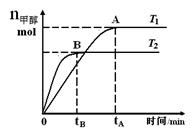
A��ƽ�ⳣ��K = 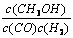
B���÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ��С
C������ʱ�̣�T2�¶��µķ�Ӧ���ʾ�����T1�¶��µ�����
D������A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱ ����
����
�ο��𰸣�D
���������A�����������Ӧ֪���÷�Ӧ��ƽ�ⳣ��K =c(CH3OH)/c(CO)c2(H2) ������B�������ͼ���֪���¶�ΪT1ʱ��ƽ��ʱ�״������ʵ�����T2ʱ�ʸ÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ�Ĵ���C��Ӱ�췴Ӧ���ʵ�����������¶ȣ�������ʱ�̣�T2�¶��µķ�Ӧ���ʾ�����T1�¶��µ����ʣ�����D�������ͼ��֪������A��ķ�Ӧ��ϵ��T1�䵽T2��ƽ�������ƶ����ﵽƽ��ʱ ������ȷ��
������ȷ��
�����Ѷȣ�һ��
2������� �����ٷɻ�β���е�NO���ƻ������㣮��ѧ�������о����ô�������β���е�NO��COת��ΪCO2��N2����ѧ����ʽ���£�
2NO+2CO
2CO2+N2 ��H��0��
Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��������崫������ò�ͬʱ���NO��COŨ�����±���
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5
c��NO��/mol?L-1
1.00��10-3
4.50��10-4
2.50��10-4
1.50��10-4
1.00��10-4
1.00��10-4
c��CO��/mol?L-1
3.60��10-3
3.05��10-3
2.85��10-3
2.75��10-3
2.70��10-3
2.70��10-3
|
��ش����¸�����������¶ȱ仯�Դ�Ч�ʵ�Ӱ�죩��
��1��ǰ2s�ڵ�ƽ����Ӧ����v��N2��=______��
��2���ڸ��¶��£���Ӧ��ƽ�ⳣ��K=______��
��3�����¶Ⱥ�������ֲ���������£��ܹ�˵���÷�Ӧ�ﵽƽ��״̬�ı�־��______��
A����Ӧ������������ʵ���Ũ�����
B��NO��CO��CO2��N2������֮��Ϊ2��2��2��1
C�����������ܶȱ��ֲ���
D����λʱ��������1molNO��ͬʱ������1molCO����
��4���ﵽƽ������������NOת���ʵ���______��
A��ѡ�ø���Ч�Ĵ���B�������������������뺤������ѹǿ
C�����ͷ�Ӧ��ϵ���¶�D����С���������
��5����Ӧ2NO+O2�T2NO2 ��S��0���Է����е�ԭ����______��
��6����Һ̬�£�N2H4����Һ̬˫��ˮ��Ϸ�Ӧʱ������������������ˮ���������ų��������ȣ���֪0.4molҺ̬����������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�256.6kJ���������÷�Ӧ���Ȼ�ѧ����ʽ��______��
��ijȼ�ϵ��������Ϊȼ�ϣ�д�����Խ������²��뷴Ӧ�ĵ缫��Ӧʽ��______��
�ο��𰸣���1����ǰ2s�ڵ�ƽ����Ӧ�ٶ�v��NO��=1.00��10-3-2.5��10-42s=3.75��10-4mol/��L?s������v��N2����v��NO��=1��2�õ�v��N2��=1.875��10-4mol/��L?s����
�ʴ�Ϊ��1.875��10-4mol/��L?s����
��2���ɱ����е����ݿ�֪��4sʱ�ﵽ��ѧƽ�⣬��
2NO+2CO����
���������
�����Ѷȣ���
3��ѡ���� �����¶ȣ��������ݲ�һ���������
A����ѧ��Ӧ����v
B��ˮ�����ӻ�����Kw
C����ѧƽ�ⳣ��K
D��������ʵĵ���ƽ�ⳣ��Ka
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
4������� ��4�֣���֪2NH3(g)  ?N2(g) +3 H2(g)?����ij�¶��£���2 L�ܱ������м���һ������NH3����Ӧ��10����ʱ����ֵ�Ũ�Ȳ��ٸı䣬��ʱ��ø���ֵ�Ũ�����£�
?N2(g) +3 H2(g)?����ij�¶��£���2 L�ܱ������м���һ������NH3����Ӧ��10����ʱ����ֵ�Ũ�Ȳ��ٸı䣬��ʱ��ø���ֵ�Ũ�����£�
����
| NH3
| N2
| H2
|
���ʵ�����mol��
| 0. 1
| 0.2
| 0.6
|
��ʱ����ƽ����Ӧ����v(N2) ��?
�ﵽƽ��״̬������˵����ȷ���ǣ�?
a��ͨ���ı䷴Ӧ ������ʹ����ƽ���ƶ�
������ʹ����ƽ���ƶ�
b��NH3�ķֽ����ʺͺϳ��������
c��NH3���ٷֽ���
d��ͨ���ı䷴Ӧ������ʹNH3ȫ���ֽ��N2��H2
�ο��𰸣�0.01moll-1min-1??ab
�����������
�����Ѷȣ�һ��
5��ѡ���� ���ڷ�ӦM+N��P������¶�ÿ���� 10�棬��Ӧ��������Ϊԭ����3������10��ʱ����ɷ�Ӧ�� 10%��Ҫ54min�����¶���ߵ�40�棬��ɷ�Ӧ��10%��Ҫ��ʱ��Ϊ
[? ]
A.2min
B.3min
C.6min
D.9min
�ο��𰸣�A
���������
�����Ѷȣ�һ��