微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
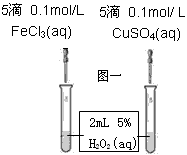
1、实验题 (1)课本设计了如图一所示实验,其目的是通过比较H2O2的分解速率来比较____________________,可通过观察_____________________________来定性比较。有同学提出将CuSO4改为CuCl2更为合理,其理由是_______________________________________________________。
(2)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你的猜想还可能是_____的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_____
A.硫酸钾
B.硫酸锰
C.水
D.氯化锰
参考答案:(1)FeCl3和CuCl2对H2O2分解的催化效果;气体产生的快慢(或用带火星的木条试验,复燃的先后);排除SO42-和Cl-不同所产生的影响
(2)催化剂(或硫酸锰或Mn2+的催化作用);B
本题解析:
本题难度:一般
2、计算题 (1)某学习小组利用下图装置制取氯气并探究其性质。
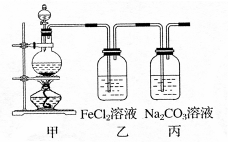
①甲装置中反应的化学方程式是?;
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象)?;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是?。
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究。
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol・L-1盐酸、品红溶液、新制澄清石灰水。
【提出假设】假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含?;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3 。
【进行实验】在答题卡上完成下表(不必检验Ca2+、Cl-):
实验步骤
| 预期现象和结论
|
①
| 用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管?
?
?
| 若无气体放出且澄清石灰水未见浑浊,则假设一成立;?
?
?
|
②
| ?
?
?
| ?
?
?
|
?
参考答案:(14分)
(1)①MnO2+4HCl (浓)  MnCl2+ Cl2↑+2H2O (2分)
MnCl2+ Cl2↑+2H2O (2分)
②KSCN溶液(1分);溶液变红色(1分)[或NaOH溶液,红褐色沉淀等合理答案均给分];
③Cl2+2H2O+Na2CO3=" NaCl+" NaCl+2NaHCO3(2分)
(2)CaCO3、CaCl2(2分)
(3)10-8/(a-0.1) (2分)
实验步骤
预期现象和结论
①
加入适量1mol/L-1盐酸(1分),塞上带导管的单孔塞,将导管另一端插入A试管中(1分)
若有气体放出且澄清石灰水未见浑浊,则假设二或三成立[或假设三不成立] (1分)
②
用胶头滴管向上述步骤后的B试管中滴入几滴品红溶液,震荡(1分)[或另取少量样品于试管中,滴入几滴蒸馏水震荡,再滴入品红溶液]
若品红不褪色,则假设二成立(1分);若品红褪色,假设三成立(1分)
本题解析:
(1)①实验室制取氯气的反应:MnO2+4HCl (浓)  MnCl2+ Cl2↑+2H2O。②FeCl2溶液与Cl2发生氧化还原反应生成三价铁离子,加入KSCN溶液,溶液变红色。③由题意得:Cl2+2H2O+Na2CO3=" NaCl+" NaCl+2NaHCO3。
MnCl2+ Cl2↑+2H2O。②FeCl2溶液与Cl2发生氧化还原反应生成三价铁离子,加入KSCN溶液,溶液变红色。③由题意得:Cl2+2H2O+Na2CO3=" NaCl+" NaCl+2NaHCO3。
(2)漂白粉主要成分CaCl2、Ca(ClO)2,Ca(ClO)2变质会生成CaCO3。提出假设二:该漂白粉全部变质,含CaCO3、CaCl2。根据假设可知检测CaCO3的实验方案。
本题难度:一般
3、选择题 下列实验不能达到目的的是(? )
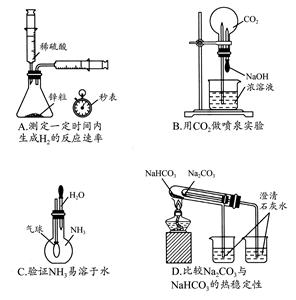
参考答案:D
本题解析:在比较Na2CO3和NaHCO3的热稳定性的实验中,因Na2CO3比NaHCO3稳定,应将NaHCO3放在里面的小试管中(温度低,还能先分解,说明不稳定),故D错。
本题难度:一般
4、实验题 (10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。
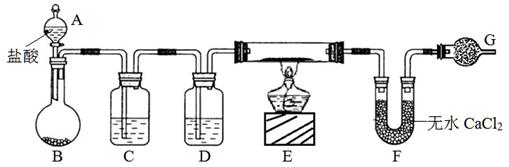
请回答:
(1)仪器中装入的试剂:D?。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是?(填序号),在这两步操作之间还应进行的操作是:?。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1:?;计算式2:?。
参考答案:(1)浓硫酸(1分)
(2)①(1分)收集G处的气体检验纯度(2分)
(3)偏小(2分)
(4)5(a-b)/m(2分) 40n/9m(2分)
本题解析:(1)由于生成的氢气中含有水蒸气,会干扰后面的实验,所以D中的盛放的应该是浓硫酸,用来除去水蒸气。
(2)由于装置中含有空气,所以应该首先生成氢气,将装置中的空气排尽。氢气是可燃性气体,再点燃之前,需要收集G处的气体检验纯度。
(3)若实验中有部分CuO被还原为红色的Cu2O,则生成的水就减少,因此氧化铜的质量分数就减少。
(4)根据方程式H2+CuO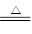 Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是
Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是 ,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是
,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是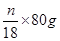 ,所以氧化铜的质量分数是40n/9m。
,所以氧化铜的质量分数是40n/9m。
本题难度:一般
5、实验题 某学习小组在实验室模拟侯氏制碱法制备纯碱,其实验流程如下:
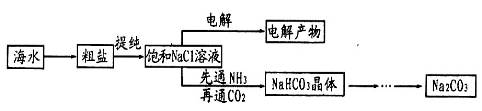
请回答下列问题:
(1)食盐溶液中含SO42-等杂质,不能用于除去SO42-的试剂是_________(填序号)。
a. Ba(OH)2? b.Ba(NO3)2? c. BaCl2? d. Na2CO3
(2)实验制备碳酸氢钠用到下列装置:

①实验装置中各接口的连接是d接____,e接_____,c接f。实验过程中先通入氨气的原因_____________。
②析出晶体后的溶液中含有大量的NH4+,检验NH4+的方法是__________________。
③瓶g内的溶液是___________________________________________。
(3)由碳酸氢钠制备纯碱的过程中用到的主要仪器除酒精灯、泥三角、三脚架、玻璃棒外,还有__________。
(4)用图电解饱和NaC1溶液的方法来制取NaOH、C12和H2。

①反应中生成的C12从_______(填“A”或“B”)放出,检验C12所用试剂(用品)______________________。
②经过长时间电解后,向电解液中滴加酚酞试液,发现溶液并未变红色,试分析可能的原因__________。
参考答案:(14分)(1)bd(2分) (2)①b? a(2分);氨气溶解度大,先通入氨气使溶液显碱性,增大CO2的吸收量,增大HCO3-的浓度(2分)?②取适量溶液于试管中,加入浓NaOH溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变蓝(2分) ③饱和碳酸氢钠溶液
(3)坩埚、坩埚钳(1分)(未答出坩埚钳不给分)
(4)①B(1分);淀粉碘化钾溶液或湿润的淀粉碘化钾试纸(1分)
②电解生成的氯气会与NaOH充分反应,导致电解最终产物仅是NaClO和H2。NaClO具有强氧化性,将酚酞氧化,故溶液不变红色(2分)
本题解析:(1)由于在除杂时不能再引入新的杂质,所以要除去食盐溶液中含有SO42-等杂质,可以选择氢氧化钡或氯化钡,而不能选择硝酸钡或碳酸钡,答案选bd。
(2)①根据装置特点可知,A装置是制备碳酸氢钠的,B装置是制备CO2的,C装置是制备氨气的,D装置是吸收多余的氨气。由于氨气极易溶于水,所以氨气要通过a口通入到装置A中,所以正确连接顺序是d接b,e接a,c接f。由于氨气溶解度大,先通入氨气使溶液显碱性,增大CO2的吸收量,从而增大HCO3-的浓度,便于碳酸氢钠晶体析出。
②铵盐能和强碱反应生成氨气,可以通过检验氨气来检验NH4+,所以正确操作是取适量溶液于试管中,加入浓NaOH溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变蓝。
③由于盐酸易挥发,所以生成的CO2中含有氯化氢,而氯化氢能和氨气反应,所以小于除去CO2中的氯化氢气体,因此瓶g内的溶液是饱和碳酸氢钠溶液。
(3)碳酸氢钠加热分解即生成碳酸钠,而固体加热需要在坩埚中进行,所以还缺少的仪器是坩埚和坩埚钳。
(4)①根据装置图可知,A和电源的负极相连,做阴极,溶液中的氢离子放电生成氢气。B和电源的正极相连,做阳极,溶液中的氯离子放电生成氯气,所以氯气在B电极生成。氯气具有强氧化性,能使湿润的淀粉碘化钾试纸变蓝色,据此可以检验氯气,因此检验C12所用试剂(用品)是淀粉碘化钾溶液或湿润的淀粉碘化钾试纸。
②由于电解生成的氯气会与NaOH充分反应,因此长时间电解后会导致电解最终产物仅是NaClO和H2。NaClO具有强氧化性,将酚酞氧化,故溶液不变红色。2和氨气的制备;仪器的选择;NH4+和氯气的检验;电解饱和食盐水的有关判断等
本题难度:困难