微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
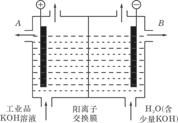
①该电解槽的阳极反应式是____________________________.
②通电开始后,阴极附近溶液pH会增大,请简述原因
③除去杂质后的氢氧化钾溶液从溶液出口_________________(填写“A”或“B”)导出
参考答案:(11分)⑴①2H+ + 2e - = H2↑ 放出气体,溶液变红。
②2Cl - - 2e - = Cl2 ↑ 析把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
⑵①纯铜 Cu2+ + 2e - = Cu ②粗铜Cu - 2e - = Cu2+
(3)①4OH--4e-=O2↑+2H2O ,②2H+ + 2e - = H2↑使H+浓度减小 ③B
本题解析:(1)①X和电源的负极相连,做阴极,溶液中的氢离子放电生成氢气,电极反应式是2H+ + 2e - = H2↑。由于随着氢离子的不断放电,阴极周围水的电离平衡被破坏,所以阴极周围溶液显碱性,溶液变成红色。
②Y电极和电源的正极相连,做阳极,溶液中的氯离子放电生成氯气,电极反应式是2Cl - - 2e - = Cl2↑。由于氯气具有强氧化性,能把碘化钾氧化生成单质碘,据此可以检验,即析把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
(2)粗铜精炼时,粗铜做阳极,纯铜做阴极,硫酸铜做电解质溶液,所以X是纯铜,电极反应式是Cu2+ + 2e - = Cu。Y电极是粗铜,电极反应式是Cu - 2e - = Cu2+。
(3)①阳极是溶液中的OH-离子放电生成氧气,电极反应式是4OH--4e-=O2↑+2H2O。
②阴极氢离子放电失去氢气,电极反应式为2H+ + 2e - = H2↑。由于随着氢离子的不断放电,阴极周围水的电离平衡被破坏,使H+浓度减小,OH-浓度增大,溶液显碱性。
③由于阳离子交换膜只能允许阳离子通过,而OH-在阴极生成。根据装置图可知,B电极是阴极,所以除去杂质后的氢氧化钾溶液从溶液出口B导出。
考点:考查电解原理的综合应用
点评:电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。
本题难度:困难
2、填空题 如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极.若A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1,合闭K2、K3通直流电,回答下列问题:
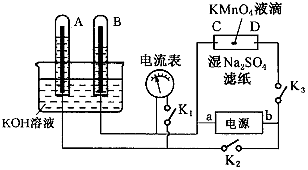
(1)判断电源的正、负极:a为________极,b为________极。
(2)在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象__________________。
(3)写出电极反应式:A极________________, C极_________________ 。
(4)若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3,合闭K1,则电流表的指针是否移动(填是或否)________。说明理由_______________ 。
参考答案:(1)负;正
(2)紫色向D方向移动,两极有气体产生
(3)4OH--4e=2H2O+O2↑;4H++4e-=2H2↑
(4)是;组成氢氧燃料电池
本题解析:
本题难度:一般
3、选择题 如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是

A.a 为电源的正极
B.通电一段时间后,石墨电极附近溶液先变红
C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑
D.电解饱和食盐水的总反应是:
参考答案:D
本题解析:Fe极做阴极,a是负极,H+发生还原反应,产生H2和NaOH;石墨做正极,Cl-发生氧化反应,产生Cl2;答案选D。
本题难度:一般
4、填空题 (15分)(1)从NaCl、CuSO4两种电解质中选取适当的物质,按电解要求填写(填化学式):
①以铜为电极,进行电解时电解质浓度不变,则采用的电解质是__________。
②以碳棒为电极,进行电解时使电解质和水的质量均变小,则采用的电解质是________。
此电解反应的阳极反应式: ,电解池的总反应化学方程式: 。
(2)①甲同学用直流电源、碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)===CuSO4+H2↑,则该同学选用的阳极材料是_______。
②乙同学在做铜与稀硫酸的上述反应实验时,看到碳棒和铜棒上都有气泡产生,但铜棒却没有被腐蚀。请你选出最可能的原因 (填字母代号)
A.铜被稀硫酸钝化 B.碳棒和铜棒与电源正负极接反
此时的电解池的总反应为____________ ____________
参考答案:(15分)(1)①CuSO4 (2分)
②NaCl (2分) 2Cl--2e-=Cl2↑(2分)
2NaCl+2H2O 2NaOH+H2↑+Cl2↑(3分)
2NaOH+H2↑+Cl2↑(3分)
(2)①铜棒 (2分)
②B(2分) 2H2O 2H2↑+O2↑
2H2↑+O2↑
本题解析:(1)①以铜为电极,进行电解时,电极氯化钠溶液,阳极是Cu失去电子生成铜离子进入溶液,阴极是氢离子放电生成氢气,氯化钠的浓度增大;而电解硫酸铜溶液,阳极是Cu失去电子进入溶液,阴极是铜离子得到电子生成单质铜析出,所以硫酸铜的浓度基本不变,所以选择CuSO4;
②以碳棒为电极,进行电解时,电解氯化钠溶液,阴极是水电离产生的氢离子放电生成氢气,阳极是氯离子放电生成氯气,则溶液中的水和氯化钠的质量都减小;电解硫酸铜溶液,阴极是铜离子放电生成单质铜,阳极是氢氧根离子放电,产生氧气,所以溶液中的硫酸铜与水的质量都减少,二者均符合题意,答案是NaCl、CuSO4;阳极的反应式为2Cl--2e-=Cl2↑或2H2O-4e-= O2↑+4H+;总反应方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑或2 CuSO4+2H2O
2NaOH+H2↑+Cl2↑或2 CuSO4+2H2O 2 H2SO4+O2↑+2Cu;
2 H2SO4+O2↑+2Cu;
(2)①Cu+H2SO4(稀)===CuSO4+H2↑该反应一般不会实现,但在电解时用Cu作阳极,稀硫酸作电解质溶液,则该反应会发生;
②首先Cu与稀硫酸不会发生钝化,当电源的正负极接反时,Cu作阴极,则Cu不会参加反应,该反应实质是电解水,答案选B;电解水的化学方程式为2H2O 2H2↑+O2↑ 。
2H2↑+O2↑ 。
考点:考查电化学原理的应用,实验现象的分析与判断
本题难度:困难
5、填空题 由软锰矿(主要成分为MnO2)制备KMnO4的实验流程可表示如下:
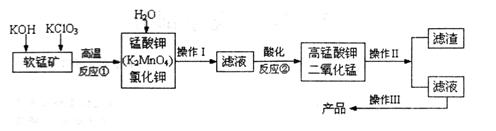
(1)操作Ⅱ的名称是____________。
(2)可循环利用的物质____________(填化学式)。
(3)反应②的产物中,氧化产物与还原产物的物质的量之比是______。
(4)反应②中“酸化”时不能选择下列酸中的______(填字母序号)
A.稀盐酸?B.稀硫酸?C.稀醋酸
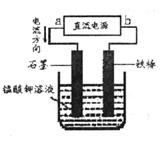
(5)电解猛酸钾溶液也可以得到高锰酸钾,其阴极反应式为:2H2O+2e-=2OH-+H2↑,如下图,b作____________极,电解池的阳极反应式是____________;若电解过程中收集到2.24L H2(标准状况),则得到高锰酸 钾____________克。(提示:阴离子放电顺序MnO42->OH-)
参考答案:(16分)
(1)过滤?(2分)
(2)MnO2?(2分)
(3)2:1?(2分)
(4)A?(2分)
(5)负?(2分),MnO42-―e-=MnO4-?(3分);31.6?(3分)
本题解析:工艺流程题解题的关键是要搞清楚加入什么物质,发生什么反应,如何分离等,通过分析,我们要能够将一个工艺的流程转化为物质的流程。第一步,KOH和KClO3与MnO2反应,得到K2MnO4,从而可以写出反应方程式为6KOH+3MnO2+KClO3=3K2MnO4+KCl+3H2O,然后加入水溶解分离可溶性物质,得到K2MnO4和KCl;第二步,将滤液酸化,得到高锰酸钾和二氧化锰,为一歧化反应,锰从+6变为+7和+4;反应方程式为3MnO42-+4H+=2MnO4-+MnO2+2H2O,通过过滤分离MnO2和高锰酸钾溶液,最终得到产品。整个过程中MnO2可以循环利用。
(4)因锰酸根和高锰酸根均具有强氧化性,不能使用盐酸(具有还原性);
(5)铁为活性电解,这里没有参与反应,做阴极故与负极相连。阳极发生氧化反应,锰酸根失电子生成高锰酸根,根据电子得失守恒可以进行相关计算。
本题难度:困难