微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 0.2L?1mol?L-1的FeCl3与0.1L?2mol?L-1的KCl溶液中,Cl-的物质的量浓度之比为
A.1:2
B.3:1
C.3:2
D.1:1
参考答案:C
本题解析:分析:先根据溶液中氯离子的物质的量浓度=盐的浓度×化学式中氯离子个数,求出各溶液中Cl-的物质的量浓度,然后求比值.
解答:0.2L?1mol?L-1的FeCl3溶液中Cl-的物质的量浓度为1mol?L-1×3=3mol?L-1,0.1L?2mol?L-1的KCl溶液中Cl-的物质的量浓度为2mol?L-1,Cl-的物质的量浓度之比为3:2,故选:C.
点评:本题考查了溶液中氯离子物质的量浓度的计算,溶液中氯离子的物质的量浓度为盐的浓度与化学式中离子个数的积,与溶液的体积无关.
本题难度:困难
2、选择题 下列实验操作,其中正确的是
[? ]
A.蒸发操作时,应将溶液放入坩埚中加热,直到完全蒸干后停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:BC
本题解析:
本题难度:简单
3、选择题 海水晒盐的原理(?)
A.利用热蒸发浓缩海水达饱和并进一步结晶
B.通过降温降低食盐的溶解度使食盐析出
C.利用加入沉淀剂的方法是食盐沉淀析出
D.利用泥沙使海水达到饱和,然后利用日光使食盐析出
参考答案:A
本题解析:由于食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用蒸发溶剂的方法。故选A。
本题难度:简单
4、选择题 下列实验中,不能达到目的是( )
A.
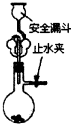
实验室用大理石与盐酸制取CO2
B.

制取SO2并检验SO2的漂白性
C.
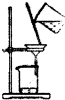
分离淀粉胶体和泥沙的混合物
D.
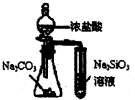
比较绿碳硅三种元素的非金属性强弱
参考答案:A.大理石与盐酸反应生成CO2,安全漏斗可防止烧瓶内压强过大导致酸液飞溅,故A正确;
B.浓硫酸和铜在加热条件下制备二氧化硫气体,二氧化硫具有漂白性,能是品红褪色,该装置可制取SO2并检验SO2的漂白性,故B正确;
C.胶体可通过滤纸,但泥沙不能透过滤纸,分离淀粉胶体和泥沙的混合物可用过滤的方法,故C正确;
D.比较非金属性强弱应用最高价含氧酸,不能用盐酸,应用高氯酸,故D错误.
故选D.
本题解析:
本题难度:一般
5、选择题 只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液,这种试剂是(?)
A.Ba(NO3)2
B.H2SO4
C.NaOH
D.AgNO3
参考答案:C
本题解析:只有NaOH 与四种试剂混合后的现象不同:
与Na2SO4不反应无现象;与MgCl2有白色沉淀生成;与FeCl2有白色沉淀生成,但迅速转化为灰绿色,最终为红褐色;与Al2(SO4)3有白色沉淀生成,但随着加入NaOH的增多,沉淀又会溶解,故答案为C
本题难度:一般