| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《盐类水解的原理》考点巩固(2017年最新版)(六)
参考答案:B 本题解析:根据溶液的电中性原理可知A项正确;若b=2a,混合后的溶液为等物质的量浓度的MCl和HCl的混合溶液,M+离子部分水解,故c(H+)>c(M+),B项错误;若a=2b,混合后的溶液为等物质的量浓度的MCl和MOH的混合溶液,因MOH的电离程度大于M+的水解程度,故c(OH-)>c(H+),MOH的电离是微弱的,故c(Cl-)>c(OH-),C项正确;若b=a,混合后的溶液为MCl溶液,根据质子守恒可知c(H+)=c(OH-)+c(MOH),D项正确 本题难度:一般 3、填空题 (10分)
参考答案:(1) FeCl3 + 3H2O 本题解析:(1)氯化铁在沸水中水解制备胶体,制备反应为FeCl3+3H2O 本题难度:一般 4、选择题 人们把能对抗外来少量酸、碱或稍加稀释而引起溶液pH发生明显变化的作用叫做缓冲作用,具有缓冲作用的溶液叫缓冲溶液.缓冲溶液往往由弱酸与其对应的盐、多元弱酸与其对应的次级盐、弱减与其对应的盐组成.下列各组溶液不能形成缓冲溶液的是 参考答案:C 本题解析: 本题难度:一般 5、选择题 Na2CO3水溶液中存在CO2-3+H2O |
参考答案:A
本题解析:A、稀释溶液,水解平衡向左移动,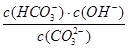 减小,A错误;B、通入CO2,由于H2CO3
减小,A错误;B、通入CO2,由于H2CO3 HCO-3+H+,溶液pH减小,B正确;C、水解是吸热过程,升高温度,此平衡常数增大,C正确;D、加入NaOH固体,CO2-3+H2O
HCO-3+H+,溶液pH减小,B正确;C、水解是吸热过程,升高温度,此平衡常数增大,C正确;D、加入NaOH固体,CO2-3+H2O HCO-3+OH-平衡向左移动,
HCO-3+OH-平衡向左移动, 减小,D正确;答案选A。
减小,D正确;答案选A。
考点:盐的水解平衡
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《盐类水解的.. | |