微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)下图是探究不同条件下化学能转变为电能的装置。请回答下列问题:
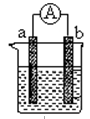
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,负极的电极反应式为:?。如果一电极质量减轻5.4 g,则另一极放出气体的体积为?L(标准状况)。
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用KOH溶液为电解液;则氢气应通入?极(填a 或b,下同),电子从?极流出。
a 极发生电极反应式为:_____________________________。
2、选择题 下列装置属于原电池的是( )
A.
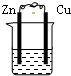
酒精
B.

CuCl2溶液
C.
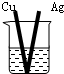
AgNO3溶液
D.

?稀硫酸? 稀硫酸
3、填空题 如下图所示装置:
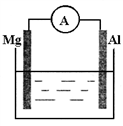
(1)若烧杯中溶液为稀硫酸,则观察到的现象为_________。两极反应式为:正极_________; 负极___________。该装置将______能转化为_________能。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为__________,总反应方程式为___________。
4、选择题 少量锌和足量的稀HCl反应时,加入少量CuSO4固体,下列叙述正确的是(D? )
A.反应速率减慢,产生H2的量不变
B.反应速率加快,产生H2的量不变
C.反应速率不变,产生H2的量略增加
D.反应速率加快,产生H2的量略减少
5、选择题 反应①?Fe(s)+CO2(g)===FeO(s)+CO(g);△H1=?a?kJ・mol-1
反应②?CO(g)+1/2O2(g)===CO2(g);△H2=?b?kJ・mol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下

(1)反应①的化学平衡常数表达式为__________,a______0(填“>”、“<”或“=”)。?在?500℃2L?密闭容器中进行反应①,Fe?和CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为__________,用CO表示的化学反应速率为_______。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有
________(填序号)。 ?
A.缩小反应器体积?B.通入CO2?C.升高温度到900℃?D.使用合适的催化剂
(3)下列图像符合反应①的是________(填序号)(图中v是速率、 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。

(4)由反应①和②可求得反应2Fe(s)+O2(g)===2FeO(s)?△H3中的△H3=_______(用含a、b的代数式表示)。
(5)如下图是甲醇燃料电池(电解质溶液为KOH溶液)的结示意图,则a处通入的是
_______(填“甲醇”或“氧气”),b处电极上发生的电极反应是:_______________。
