微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列操作达不到预期目的的是
①石油分馏时把温度计水银球插入受热的液体中;②用酸性高锰酸钾溶液除去乙炔中含有的H2S;③用溴乙烷在NaOH溶液中加热后,加入AgNO3溶液检验卤素原子;④将苯和溴水混合后加入铁粉制取溴苯;⑤将敞口久置的电石与蒸馏水混合制取乙炔
A.①⑤
B.③④⑤
C.①②③⑤
D.①②③④⑤
参考答案:D
本题解析:略
本题难度:简单
2、实验题 下面是某科学兴趣小组的同学做同周期元素性质递变规律实验时,设计的一套实验方案。其中实验步骤如下

请整理并完成实验报告。
(1)实验目的:________。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液等。仪器:①____,②______,表面皿,试管夹,镊子,小刀,玻璃片,砂纸等。
(3)实验内容:(完成下列表格中的实验现象和化学方程式,实验步骤略)
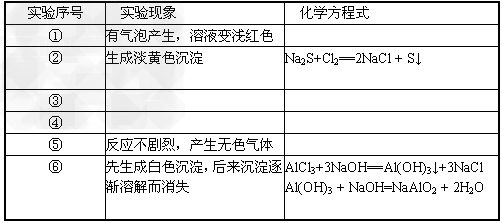
(4)实验结论:________。
(5)请用原子结构的知识简单解释上述结论:_______________。
参考答案:(1)探究同周期元素性质的递变规律?
(2)试管;酒精灯(3) 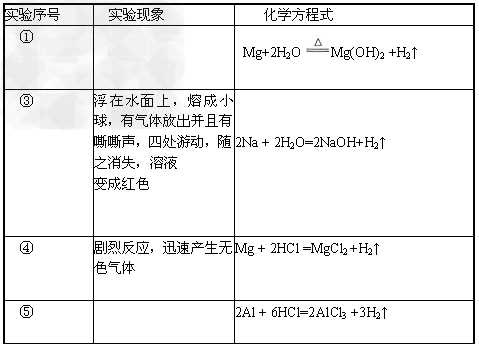 (4)同周期元素随着原子序数的递增,失电子能力逐渐减弱,得电子能力逐渐增强 ?
(4)同周期元素随着原子序数的递增,失电子能力逐渐减弱,得电子能力逐渐增强 ?
(5)同周期的元素原子电子层数相等,核电荷数逐渐增大,原子半径逐渐减小,原子核对核外电子的吸引力逐渐增强,失电子能力逐渐减弱,得电子能力逐渐增强
本题解析:
本题难度:一般
3、实验题 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)完成以下实验设计表(表中不要留空格)。

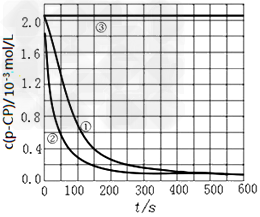
[数据处理]实验测得p―CP的浓度随时间变化的关系如图,①②③分别代表以上三组实验测得的数据曲线。
(2)请根据实验①曲线,计算降解反应在 50~150s内的平均反应速率;v(p―CP)=?
_________?mol L-1
L-1 s-1。
s-1。
(3)实验①、②表明温度升高,该降解反应速率_____。?(增大或减小)但其他文献表明,温度过高时(如接近100℃)反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:?_________________________________。
(4)实验③得出的结论是:pH等于10时,_________________________
(5)实验时需在不同时间从反应器中取样,并使所取样品中反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:_____________________________。
参考答案:(1)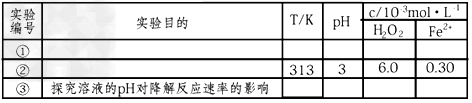 (2)8.0×10-6
(2)8.0×10-6
(3)增大;过氧化氢在温度过高时迅速分解。
(4)反应速率趋向于零(或该降解反应趋于停止)
(5)将所取样品迅速加入到一定量的NaOH溶液中,使pH约为10
本题解析:
本题难度:一般
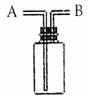
4、选择题 用下图所示装置进行如下实验,不能达到实验目的的是
?
A.瓶中盛满水,从B口进气,用排水法收集H2
?
B.瓶中盛适量浓硫酸,从A口进气来干燥CO2
?
C.从B口进气,用排空气法收集NO2
?
D.瓶中装满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成O2的体积
参考答案:C
本题解析:略
本题难度:一般
5、实验题 超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下
2NO+2CO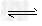 2CO2+N2
2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
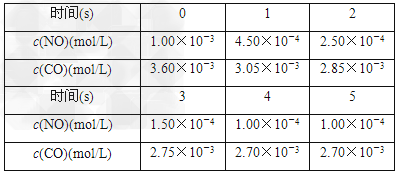
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的ΔH________0(填写“>”“<”“=”)。
(2)前2s内的平均反应速率v(N2)=________。
(3)在该温度下,反应的平衡常数K=________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A.选用?更有效的催化剂
B.升高反应体系的温度
C.降低反应体系的温度
D.缩小容器的体积
(5)研究表明:在使用等质?量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
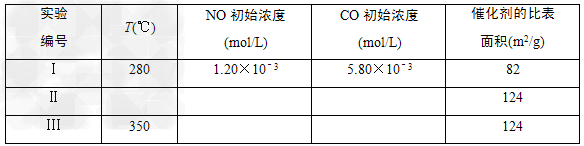
①请在上表空格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。?
参考答案:(1)<
(2)1.875×10-4?mol/(L?s)
(3)5?000
(4)C、D
(5)①Ⅱ:280 ;1.20×10-3 ;5.80×10-3 Ⅲ:1.20×10-3 ;5.80×10-3
②如图: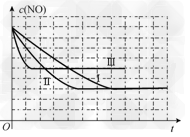
本题解析:
本题难度:困难