微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是
[? ]
A.NaOH溶液[Ba(OH)2]:用Na2SO4溶液
B.NaCl溶液(Na2SO4):用Ba(NO3)2溶液
C.KOH溶液(K2CO3):用Ca(OH)2溶液
D.HNO3溶液(HCl):用AgNO3溶液
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列不属于海水淡化方法的是:
A.蒸馏法
B.过滤法
C.电渗析法
D.离子交换法
参考答案:B
本题解析:海水淡化的主要方法是蒸馏法、电渗析法和离子交换法,过滤法不是海水淡化的方法,答案选B。
点评:该题是常识性知识的考查,难度不大,侧重对基础基础知识的巩固和训练。注意知识的积累和总结,并能熟练记住即可。
本题难度:简单
3、实验题 (8分)
(1)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分,进行以下实验:取甲溶液,向其中缓慢滴入乙溶液,并边滴加边振荡,观察到开始无明显现象,后来有大量气体生成。实验过程中所发生反应的离子方程式为:?;甲是?溶液,乙是?溶液;
(2)为了达到下表所列的实验目的,请选择合适的实验方法,将其标号填在相应的空格中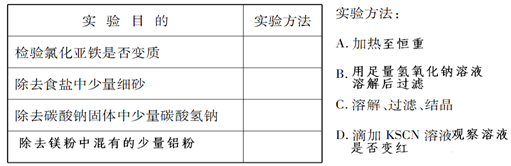
参考答案:(8分)
(1)CO32- + H+ = HCO3-? HCO3- + H+ = H2O+ CO2↑;碳酸钠,稀盐酸;
(2)
实验目的
实验方法
检验氯化亚铁是否变质
D
除去食盐中的少量细砂
C
除去碳酸钠固体中少量碳酸氢钠
A
除去镁粉中混有的少量铝粉
B
本题解析:考查物质的鉴别、分离及提纯
(1)两溶液互相滴加,所发生的离子反应不同,实验现象不同,以此可鉴别两溶液
当向碳酸钠溶液中滴加盐酸时:CO32-+H+=HCO3-? HCO3-+H+=H2O+CO2↑,故一开始无气体产生,后来才有气体生成;
当向盐酸中滴加碳酸钠学时,CO32-+2H+=H2O+CO2↑,一开始即有气体生成
(2)
氯化亚铁易被氧化为氯化铁,氧化产物铁离子可用KSCN溶液来检验
细砂不溶于水,与可溶于水的食盐可采用过滤的方法来提纯
碳酸氢钠具有热不稳定性,加热可除去,并且可生成碳酸钠
铝粉可溶于碱液,故可用NaOH溶液来除去铝粉
本题难度:简单
4、选择题 一个集气瓶的质量为20.0 g,在相同状况下,装满O2时质量为21.0 g,装满A气体时为22.0 g,则A气体的摩尔质量为
A.16 g・mol-1
B.32 g・mol-1
C.64 g・mol-1
D.128 g・mol-1
参考答案:C
本题解析:根据阿伏加德罗定律,气体质量之比等于摩尔质量之比:(21.0 g-20.0 g)/(22.0 g-20.0 g)=32 g・mol-1/M,解得:M=64 g・mol-1.
本题难度:简单
5、简答题 工业制备氯化铜时,将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3].请回答以下问题:
(1)第一步除去Fe2+,能否直接调整溶液pH=9.6,将Fe2+沉淀除去?______,(填“能”或“不能”)理由是______,
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:
①加入NaClO后,溶液的pH变化是______(填代号).
A.一定增大B.一定减小C.可能增大D.可能减小
②你认为用NaClO作氧化剂是否妥当?______,(填“是”或“否”)现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有______(有几个选几个,填代号).
A.浓HNO3B.Cl2 C.KMnO4D.H2O2
(3)加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的______.
A.NaOHB.NH3?H2OC.CuOD.Cu(OH)2.
参考答案:(1)由题给信息可知,除去Fe2+时,应避免Cu2+生成沉淀,如直接调整溶液pH=9.6,则生成氢氧化亚铁的同时,氢氧化铜、氢氧化铁也同时生成,
故答案为:不能;因Fe2+沉淀的pH最大,Fe2+沉淀完全时,Cu2+、Fe3+也会沉淀完全;
(2)①NaClO为强碱弱酸盐,水解呈碱性,则加入NaClO,溶液的pH一定增大,另外NaClO可以酸反应生成HClO而导致溶液pH增大,故答案为:A;
②加入氧化剂时,不能引入新的杂质,如用NaClO,则可引入NaCl杂质,应加入氯水或过氧化氢,
故答案为:否;BD;
(3)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质,则可用CuO 或Cu(OH)2或CuCO3;
故答案为:CD.
本题解析:
本题难度:一般