��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ӱ��ӵ��Ҵ���Һ�л��ձ��ӣ������в�����
������
�ڹ���
�۾��á���Һ
�ܼ�������������
��ͨ�������CO2
����������NaOH��Һ
����������FeCl3��Һ
�����������Ũ����������ȡ�
������ʵ�������
[? ]
A.�ܢݢ�
B.�ޢ٢ݢ�
C.���
D.��ڢݢ�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� �������ʵ��Ʊ�������ȷ����
A��Al��OH��3��������Ӧ
B��Al���������AlCl3
C��������Һ����������Һ���백ˮ��
D�������飺��������ˮ��Ӧ
�ο��𰸣�A
���������AlCl3Ϊ���ۻ��������AlCl3�����磬����⣻������Һ����Ӧ�Ѱ�ˮ������������Һ������ǡ����ʧ��������������ˮ����ȡ����Ӧ��Ӧ��Һ����������������Թ��ա�
�����Ѷȣ���
3��ѡ���� ��ͼ��ʾ�ӻ�����з����X�����ַ��������ݷ���I�ͷ�����ָ������˵����������
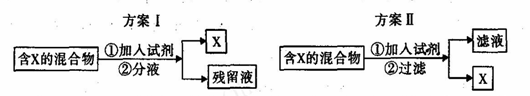
A������X�Ļ����Ϊ��ˮ����ͨ������I���з��룬�����Լ�ΪCC14Һ�壬�����Һ��ֲ㣬�ϲ�ΪX��CC14��Һ
B������X�Ļ����Ϊ���ͱ��ӣ���ͨ����������з��룬�����Լ�ΪŨ��ˮ��XΪ���屽��
C������X�Ļ����Ϊ������Ӧ��Ļ�����ͨ������I���з��룬�����Լ�Ϊ����ʳ��ˮ������Һ�к��и���
D������X�Ļ����ΪFe��Al����ͨ������II���з��룬�����Լ�Ϊ����NaOH��Һ��1mol X������������ȫ��Ӧʱ��ת��3mol����
�ο��𰸣�D
���������A����CC14��ȡ��ˮ������CC14���ܶȴ���ˮ���ֲ��ˮ�����Ϸ���CC14λ���²�
B�����뱽�ͱ��ӣ�������Ũ��ˮ����ʹ���뱽�ӷ�Ӧ���������屽���ڱ���Ҳ�����Գ����ķ�ʽ���ڣ����������л��Լ����У����뱽�ͱ��ӣ�һ���Ǽ���NaOH��Һ���ٷ�Һ��
C��������Ӧ��Ļ���һ���Ǽ���ʳ��ϸ���������������ٽ��й��˷��롣
D��������������ǿ����Һ�����ʣ��������������ȷ��
�����Ѷȣ�һ��
4��ѡ���� ͬ��ͬѹ�£�25?mL����A2��50?mL����B2��Ӧ������25?mL?C��������C�Ļ�ѧʽΪ
A.AB2
B.A2B
C.A2B4
D.AB
�ο��𰸣�C
���������ͬ��ͬѹ�£�����ʽ�еĻ�ѧ������֮�ȵ��ڷ�Ӧ��ϵ�еĸ��������֮�ȣ�����A2��2B2====C���־������غ㶨�ɣ�ԭ�Ӹ����غ㶨�ɣ���֪C�Ļ�ѧʽΪA2B4������ѡC��
�����Ѷȣ�����
5������� ���ݷ�ˮ�������к����ʵIJ�ͬ����ҵ���ж��ַ�ˮ�Ĵ���������
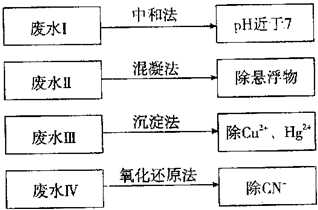
��1���ٷ�ˮI������CO2���������ӷ���ʽ��______��
�ڷ�ˮ��������������ʵ���з��ַ�ˮ�е�c��HCO-3��Խ��ˮЧ��Խ�ã�������Ϊ______��
�۷�ˮ���еĹ�Ԫ�ش�������ת�����ڿո�������Ӧ�Ļ�ѧʽ����Hg2++______�TCH3Hg++H+
�ҹ��涨��Hg2+���ŷű����ܳ���0.05mg/L����ij�����ŷŵķ�ˮ1L�к�Hg2+3��10-7mo1���Ƿ�ﵽ���ŷű�______����ǡ�����
�ܷ�ˮ������Cl2����CN-��CO2��N2�����μӷ�Ӧ��Cl2��CN-�����ʵ���֮��Ϊ5��2����÷�Ӧ�����ӷ���ʽΪ______��
��2����ѧ��������COD��������ˮ�����л�����Ⱦ�ij̶ȣ�����ָ��һ�������£���ǿ����������ˮ��ʱ�����ĵ�����ɲ��������������ĺ�������mg/L�ƣ���ij�о���ѧϰС��ⶨijˮ���Ļ�ѧ��������COD�����������£�
��ȡV1 mLˮ������ƿ������10.00mL?0.2500mol/L?K2Cr2O7��Һ��
�����Ƭ������Ȼ���������������ữ����Ͼ��ȣ����ȣ�
��Ӧ��Ϻ���ȴ����ָʾ������c?mol/L�����������[��NH4��2Fe��SO4��2]��Һ?�ζ����յ�ʱ���������������ҺV2?mL��
��I�У���ȡK2Cr207����Һ��������______��
�ڢ��У����Ƭ��������______��
�ۢ��У������ķ�ӦΪ��Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3+7H2O�ɴ˿�֪����ˮ���Ļ�ѧ������COD=______���ú�c��V1��V2�ı���ʽ��ʾ����
�ο��𰸣���1����pH�ӽ�7����CO2����������HCO3-����Ӧ�����ӷ���ʽΪOH-+CO2=HCO3-���ʴ�Ϊ��OH-+CO2=HCO3-��
��HCO3-��Al3+������ٽ���ˮ�⣬����CO2��Al��OH��3���Ӷ���ǿ��ˮЧ����
�ʴ�Ϊ��HCO3-��ٽ�Al3+��ˮ�⣬���ɸ����Al��OH��3����ˮЧ����ǿ��
�۸��ݵ���غ�������غ��֪��ӦΪHg2+��CH4�ķ�Ӧ��
1Lˮ�У�n��Hg2+��=3��10-7mo1����m��Hg2+��=3��10-7mo1��200.6g/mol=6.02��10-5g=0.06mg��0.05mg������û�дﵽ�ŷű����ʴ�Ϊ��CH4����
�ܷ�ˮ������C12����CN-��CO2��N2�����μӷ�Ӧ��C12��CN-�����ʵ���֮��Ϊ5��2��
��Ӧ�����ӷ���ʽΪ5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+���ʴ�Ϊ��5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+��
��2����K2Cr207����ǿ�����ԣ�Ӧ����ʽ�ζ��ܻ���Һ����ȡ�����ü�ʽ�ζ��ܣ��ḯʴ�ܣ��ʴ�Ϊ����ʽ�ζ��ܣ�����Һ�ܣ���
�����Ƭ��ֹ���е����ã��ʴ�Ϊ����ֹ���У�
��n��K2Cr2O7��=0.01L��0.2500mol/L=2.5��10-3mo1��
n��Fe2+��=V2��10-3L��cmol/L=cV2��10-3mol��
��Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O��֪��
ˮ�����ĵ�n��K2Cr2O7��=2.5��10-3mo1-16��cV2��10-3mol=15-cV26��10-3mol��
�õ��ӣ�2����6-3����15-cV26��10-3mol=��15-cV2����10-3mol��
���ݵ���ת�ƣ������14����15-cV2����10-3mol������
m��O��=14����15-cV2����10-3mol��32g/mol=8����15-cV2����10-3g=8����15-cV2��mg��
���ԣ�COD=8��(15-cV2)mgV1��10-3L=8000��(15-cV2)V1mg/L��
�ʴ�Ϊ��8000��(15-cV2)V1��
���������
�����Ѷȣ�һ��