微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 2011年3月11日日本发生了9.0级强地震。福岛第一核电站1号机组12日下午发生氢气爆炸。随后在爆炸核电站周围检测到的放射性物质有碘-131和铯-137。碘-131一旦被人体吸入,可能会引发甲状腺疾病。日 本政府计划向核电站附近居民发放防止碘-131辐射的药物碘片。
(1) Cs(铯)的最外层电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素A、B、C的电离能如下表

那么三种元素A、B、C的元素符号分别为___________,形成其单质晶体的化学键类型是____________。
(2)F与I同主族,BeF2与氢气爆炸的生成物H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是________、_________。
(3)与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物,非金属氯化物等。
BCl3是一种非金属氯化物,该物质分子中B-Cl键的键角为_____________。
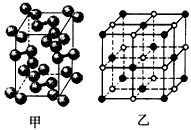
(4)碘-131是碘单质,其晶胞结构如下图甲所示,该晶胞中含有_______个I2分子;KI的晶胞结构如下图乙 所示,每个K+紧邻___个I-。
参考答案:(1)Li、Na、K;金属键
(2)sp;sp3
(3)120°
(4)4;6
本题解析:
本题难度:一般
2、填空题 水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为_____?_____;
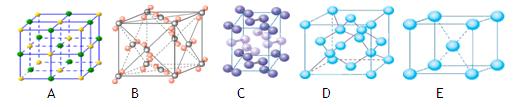
(2)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__?___(请用相应的编号填写)
(3)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是a kJ/mol,除氢键外,水分子间还存在范德华力(b kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:? ?。
?。
参考答案:每空2分,共8分。
(1)1S22S22P6?(2) BC?(3)1/2(a-b) (4)Cu2++4H2O=[Cu(H2O)4]2+
本题解析:略
本题难度:一般
3、选择题 下列有关晶体的叙述中,错误的是(?)
A.在SiO2晶体中,每个Si原子与4个O原子形成共价键
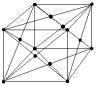
B.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
C.NaCl晶体中与每个Na+距离相等且最近的Cl―有6个;
D.CsCl晶体中与每个Cs+距离相等且最近的Cl―有8个
参考答案:B
本题解析:面心立方中,我们可以看成是以该原子为中心的三个面,每个面上有4个,共有12个。
本题难度:简单
4、选择题 共价键、离子键、分子间作用力都是粒子间的作用力,下列物质中会有以上两种作用的晶体是(?)
A.SiO2
B.Ar
C.NaCl
D.NaOH
参考答案:D
本题解析:SiO2晶体中只存在共价键;Ar是单原子分子,只存在分子间作用力;NaCl是离子晶体,只存在离子键;NaOH晶体中,Na+与OH-之间通过离子键结合,而OH-内O与H之间存在极性共价键。
本题难度:简单
5、选择题 下列分子或离子中心原子的VSEPR模型为四面体而且其空间构型为V形的是( )
A.SO2
B.NF3
C.H3O+
D.OF2
参考答案:D
本题解析:
本题难度:简单