| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《pH计算》试题巩固(2017年最新版)(二)
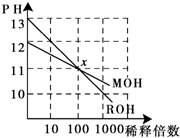 参考答案:A.由图可知,ROH的pH=13时稀释100倍,pH变为11,则ROH为强碱,故A错误; 本题解析: 本题难度:简单 3、选择题 常温下,将不同浓度的氨水与盐酸等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,则下列说法不正确的是 | |||
| 编号 | 氨水的物质的量浓度 (mol/L) | 盐酸的物质的量浓度 (mol/L) | 混合溶液的pH 第1组 0.1 0.1 pH=X 第2组 c1 0.2 pH=7 第3组 0.2 0.1 pH>7 |
参考答案:C
本题解析:
本题难度:简单
4、填空题 常温下在20mL 0.1mol.L-1 Na2CO3溶液中逐渐加入0.1mol.L-1的HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的物质的量的百分量(纵轴)也发生变化(CO2会逸出未画出),如图所示,回答下列问题: 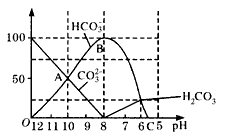
(1)随着盐酸的加入,HCO3-的浓度变化趋势是____;请写出 OAB段的离子方程式:____。
(2)当加入盐酸使溶液的pH=10时,混合溶液中含碳元素的离子有 ____,其物质的量之比是____;当pH=7时,混合溶液中含碳元素的微粒有____。
(3)在pH=____时开始逸出CO2气体,当pH=5时,逸出的气体的物质的量____0. 002mol(填“>”、“<”或“=”)。
参考答案:
(1)先增大后减小; CO32- + H+==HCO3-
(2)CO32-、HCO3- ;1:1; HCO3-、H2CO3
(3)6; <
本题解析:
本题难度:一般
5、选择题 物质的量浓度相同的盐酸和氨水,下列说法中错误的是( )
A.若混合后溶液呈中性,则有c(Cl-)=c(NH4+)
B.用湿润的pH试纸测定两溶液的pH时,氨水的误差更小
C.若混合后溶液呈中性,则所需氨水的体积小于盐酸的体积
D.两溶液等体积混合时,充分反应后:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
参考答案:A.混合溶液呈中性,则c(OH-)=c(H+),根据电荷守恒得c(Cl-)+c(OH-)=c(H+)+c(NH4+),所以c(Cl-)=c(NH4+),故A正确;
B.氯化氢是强电解质,一水合氨是弱电解质,加水稀释促进一水合氨电离,稀释相同的倍数时,氨水c(H+)或c(OH-)变化小于盐酸,所以氨水pH变化小于盐酸,则氨水的误差更小,故B正确;
C.氯化铵是强酸弱碱盐,其溶液呈酸性,要使二者混合溶液呈中性,则氨水应该稍微过量,氨水和盐酸浓度相等,所以所需氨水的体积大于盐酸的体积,故C错误;
D.盐酸和氨水的相等,两种溶液等体积混合,则二者的物质的量相等,二者恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,所以c(H+)>c(OH-),故D错误.
故选:CD.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《二氧化硫》.. | |