微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
HIn(溶液) 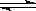 H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液)
红色?黄色
浓度为0.02 mol・L-1的下列各溶液
①盐酸②石灰水③NaCl溶液?④NaHSO4溶液?⑤NaHCO3溶液 ?⑥氨水
?⑥氨水
其中能使指示剂显红色的是
A.①④⑤
B.②⑤⑥
C.①④
D.②③⑥
参考答案:C
本题解析:略
本题难度:一般
2、选择题 在一定条件下,某密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g);ΔH=-196.6 kJ・mol-1。反应达平衡后,SO2、O2、SO3的物质的量之比为3∶2∶4,其他条件不变,升高温度,达到新的平衡时,n(SO2)=1.4 mol,n(O2)=0.9mol,则此时SO3的物质的量为
2SO3(g);ΔH=-196.6 kJ・mol-1。反应达平衡后,SO2、O2、SO3的物质的量之比为3∶2∶4,其他条件不变,升高温度,达到新的平衡时,n(SO2)=1.4 mol,n(O2)=0.9mol,则此时SO3的物质的量为
[? ]
A.1.4 mol
B.1.6 mol
C.1.8 mol
D.2.0 mol
参考答案:A
本题解析:
本题难度:一般
3、选择题 某可逆反应a A(g)+bB(g) 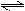 ?cC(g),在温度分别为T1和T2,压强分别为P1和P2条件下,得到C的物质的量n与时间t的关系曲线如下图所示。
?cC(g),在温度分别为T1和T2,压强分别为P1和P2条件下,得到C的物质的量n与时间t的关系曲线如下图所示。
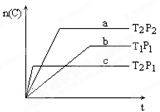
据图分析,以下正确的是
A.c>a+b,正反应为吸热反应
B.c>a+b,正反应为放热反应
C.c<a+b,逆反应为吸热反应
D.c<a+b,逆反应为放热反应
参考答案:B
本题解析:略
本题难度:一般
4、计算题 在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:
CO(g)+H2O(g) CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol。求:
CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol。求:
(1)达到平衡时CO2的物质的量分数和该反应的化学平衡常数;
(2)达到平衡后向该平衡体系中通入1.0mol水蒸气,达到新的平衡状态时,求水蒸气的物质的量和CO2的物质的量分数。
参考答案:(1)25%? 1
(2)1.33mol? 22.22%
本题解析:? CO(g)? +? H2O(g)? ?CO2(g)? +? H2(g)
?CO2(g)? +? H2(g)
起始物质的量:? 1.0mol? 1.0mol? 0? 0
转化:?x? x? x? x
平衡物质的量:? (1-x)mol? (1-x)mol? x?x
依题意可知: x=0.5mol
达到平衡时CO2的物质的量分数为:x/2=0.25=25%
该反应的化学平衡常数: 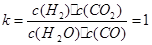
⑵? CO(g)? +? H2O(g)? ?CO2(g)? +? H2(g)
?CO2(g)? +? H2(g)
平衡时各物质的浓度:? 0.5mol? 0.5mol? 0.5mol? 0.5mol
通入1.0mol水蒸气:? 0.5mol? 1.5mol? 0.5mol? 0.5mol
转化:? y? y? y? y
再次平衡:?(0.5-y)? (1.5-y)? (0.5+y)? (0.5+y)
依据平衡常数有:
解之得: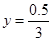
水蒸气的物质的量:n(H2O)=1.5-0.5/3=4/3mol
CO2的物质的量分数: 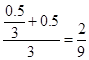
本题难度:一般
5、选择题 CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下一定达到最大限度的是
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下一定达到最大限度的是
A.CO全部转化为乙醇
B.正反应和逆反应的化学反应速率均为零
C.CO和H2以1∶2的物质的量之比反应生成乙醇
D.反应体系中乙醇的物质的量浓度不再变化
参考答案:D
本题解析:A.可逆反应的特点是反应物不可能全部转化为生成物,错误;B.化学平衡是动态平衡,达平衡时反应仍在进行,错误;C.无论是平衡还是没有平衡,CO和H2以1∶2的物质的量之比一直进行着反应,不正确。D浓度不改变,说明反应达到平衡,正确。
本题难度:一般