微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
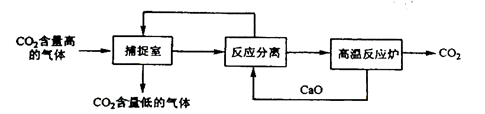
下列有关该方法的叙述中错误的是
A.能耗大是该方法的一大缺点
B.整个过程中,有两种物质可以循环利用
C.捕捉到的CO2可用来制备甲醇等产品,可减少碳排放
D.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
2、选择题 同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是
A.密度比为16∶11
B.分子个数比为16∶11
C.体积比为1∶1
D.氧原子个数比为1∶1
3、实验题 已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂;烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol・L-1 NaOH、6 mol・L-1 NaOH、0.1 mol・L-1 HCl、蒸馏水。
必要时可参考:
沉淀物
| 开始沉淀时的pH
| 沉淀完全时的pH
|
Mg(OH)2
| 9.6
| 11.1
|
Fe(OH)3
| 2.7
| 3.7
|
?
根据你设计的实验方案,叙述实验操作、预期现象和结论。(测定溶液pH的具体操作可不写)
实验操作
| 预期现象和结论
|
步骤1:
| ?
|
步骤2:
| ?
|
步骤3:
| ?
|
……
| ?
|
?
4、选择题 下列实验操作、现象和解释都正确的是
选项
| 实验操作
| 现象
| 解释
|
A.
| 向某溶液中加入盐酸
| 产生无色气体
| 溶液中一定含有CO32?
|
B.
| 新制Fe(OH)2露置于空气中一段时间
| 白色固体迅速变为灰绿色,最终变为红褐色
| 说明Fe(OH)2易被氧化成Fe(OH)3
|
C.
| 在CuSO4溶液中加入KI溶液,再加入苯,振荡
| 有白色沉淀生产,苯层呈紫色
| 白色沉淀可能为CuI
|
D.
| 向某无色溶液中滴加硝酸酸化的BaCl2溶液
| 产生白色沉淀
| 溶液中一定含有SO42-
|
?
5、实验题 某实验小组对普通锌锰废干电池内的黑色固体进行探究,设计如下方案:
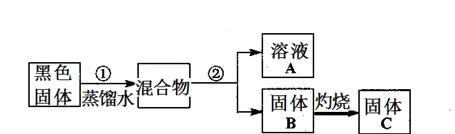
己知:I、普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。
II、氢氧化锌为白色粉末,不溶于水,溶于酸、强碱溶液和氨水。
请回答以下问题:
(1)②操作的名称是___________。
(2)某同学猜想溶液A的成分含有NH4Cl和ZnCl2,请你设计一个实验方案,验证其猜想正确,要求在答题卡上按下表格式写出实验操作、预期现象和结论。
限选试剂:蒸馏水、2moL・L-1 HCI 、2 moL・L-1 HNO3 、2 moL・L-1 NH3・H2O、6 moL・L-1 NaOH、0.1 moL・L-1 KSCN、0.1 moL・L-1 BaCl2、0.1 moL・L-1 AgNO3、紫色石蕊试液、红色石蕊试纸
实验操作
| 预期现象
| 结论
|
步骤1:各取少量溶液A分装a、b、c三支试管,往a试管,__
__________________________
| 有白色沉淀产生
| 说明溶液A含有Cl-
|
步骤2:往b试管,__________
__________________________
| ______________________
| _______________________
|
步骤3:往c试管,__________
__________________________
| 先产生_______________,
后____________________
| 说明溶液A含有Zn2+
|
?
(3)取少量固体c放入试管,滴加入双氧水,观察到有气体产生,写出该反应的化学方程式:_______________。
(4)为测定废干电池中二氧化锰的质量分数,进行下面实验:准确称取ag废千电池固体,溶于稀硫酸,加入碘化钾溶液,充分反应后,用bmol/L硫代硫酸钠标准溶液滴定,用淀粉作指示剂,滴定至终点,重复实验,平均消耗硫代硫酸钠标准溶液的体积为vmL,则废电池中二氧化锰的质量分数的计算表达式为:________________________________。
(滴定有关反应:MnO2+2I-+4H+=Mn2++I2+2H2O;I2+2S2O32-=2I-+S4O62-)