| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《原电池原理》高频考点巩固(2017年模拟版)(四)
(3)滤纸上发生的化学方程式为: 。 III.该小组同学用图乙所示装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色:停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(FeO42-)在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题: (4)电解过程中,X极溶液的pH (填“增大”“减小”或“不变”)。 (5)电解过程中,Y极发生的电极反应为4OH?-4e?=2H2O+O2↑和 。 (6)电解进行一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到气体为 mL(均已折算为标准状况时气体体积)。 参考答案:Ⅰ、负 Ⅱ(1)B (2)从右向左 (3)2NaCl + 2H2O 本题解析: 本题难度:一般 2、选择题 如图为一原电池装置,下列叙述中正确的是( ) 参考答案:A.该原电池中,铜是正极,电极反应为Cu2++2e-=Cu,铜离子在铜片表面被还原生成铜单质,故A正确; 本题解析: 本题难度:一般 3、选择题 锂钒氧化物电池的能量密度远远超过其它材料电池,其成本低,便于大量推广,且对环境无污染。电池总反应式为:V2O5+xLi==LixV2O5。下列说法中,不正确的是 参考答案:A 本题解析: 本题难度:一般 4、选择题 铜锌原电池(如图)工作时,下列叙述正确的是 ( ) |
参考答案:B
本题解析:A.Zn为活泼金属,作负极, 故Zn-2e-===Zn2+是负极反应式;B.电池反应为:Zn+Cu2+===Zn2++Cu,正确;C.在外电路中,电流从正极流向负极,电子从负极流向正极,原说法错误;D.根据溶液电荷守恒,盐桥中的K+移向消耗Cu2+的CuSO4溶液中,原说法不正确。
考点:盐桥电池的工作原理。
本题难度:一般
5、选择题 下列叙述正确的是
A.在pH=1的溶液中,Cu2+、Fe2+、NO3-和SO42-能大量共存
B.用惰性电极电解饱和氯化钠溶液的离子方程式:2Cl- + 2H+ = H2↑+ Cl2↑
C.镁铝合金被碱液腐蚀时,负极反应式为:Mg ― 2e- = Mg2+
D.大量使用含磷洗涤剂会造成水体富营养化
参考答案:D
本题解析:A.pH=1的溶液显酸性,则Fe2+与NO3-发生氧化还原反应,不能大量共存,A错误;B.用惰性电极电解饱和氯化钠溶液的离子方程式为:2Cl- + 2H2O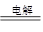 H2↑+ Cl2↑+2OH―,B错误;C.镁铝合金被碱液腐蚀时,铝与碱液反应,则负极反应式为:Al ― 3e- +4OH―=AlO2―+2H2O,C错误;D.磷元素是植物生长的必需元素,因此大量使用含磷洗涤剂会造成水体富营养化,D正确,答案选D。
H2↑+ Cl2↑+2OH―,B错误;C.镁铝合金被碱液腐蚀时,铝与碱液反应,则负极反应式为:Al ― 3e- +4OH―=AlO2―+2H2O,C错误;D.磷元素是植物生长的必需元素,因此大量使用含磷洗涤剂会造成水体富营养化,D正确,答案选D。
考点:考查离子共存、电化学原理以及水体富营养化
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《物质的分离.. | |