| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《原电池原理》高频考点巩固(2017年模拟版)(六)
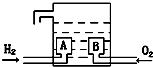 参考答案:A.氢氧燃料电池工作时,通入氢气的一极为电池的负极,发生氧化反应,故A正确; 本题解析: 本题难度:一般 2、选择题 下列实验装置符合实验目的是( )
A.A B.B C.C D.D 参考答案:A.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,电解质溶液为可溶性的硫酸铜溶液,故A错误; 本题解析: 本题难度:简单 3、选择题 下列与装置有关的说法正确的是 参考答案:D 本题解析:A、图a是电解池,铁和电源的正极相连,作阳极,失去电子。碳棒是阴极,溶液中的氢离子在阴极放电,生成氢气,因此随着电解的进行溶液中H+的浓度越来越小,A不正确;B、图b是原电池,Mg的金属性强于铝的金属性,但镁和氢氧化钠溶液不反应,铝和氢氧化钠溶液反应,所以铝电极作电池的负极,镁电极是正极,B不正确;C、图c是原电池,根据正负极可知,Cd是负极,失去电子。Co是正极,溶液中的Co2+达到电子,因此发生的反应为Cd+Co2+= Co+Cd2+,C不正确;? D、图d中:K分别与M、N连接,Fe电极分别作阴极和正极,所以均受到保护不会腐蚀,D正确,答案选D。 本题难度:一般 4、简答题 如图,氢氧燃料电池已用于宇宙飞船及潜水艇中,其电极反应为:负极:2H2-4e-+4OH-=4H2O?正极:O2+2H2O+4e-=4OH-所产生的水可作为饮用水,今欲得常温下1L这样的水,则电池内转移电子的物质的量大约是______mol. 参考答案:1L水的质量为1000g,水的物质的量为n=mM=1000g18g/mol=5009mol 本题解析: 本题难度:一般 5、选择题 研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是 参考答案:A 本题解析:A、根据题给电池反应知,每生成1mol?Na2Mn5O10转移2mol电子,正确;B、在原电池的正极上发生得电子的还原反应,电极反应式为5MnO2+2e-=Mn5O102-,错误;C、Na+不断向“水”电池的正极移动,错误;D、在反应中,银元素化合价升高,AgCl是氧化产物,错误。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《物质的分离.. | |