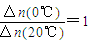微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
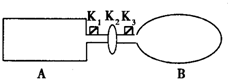
1、简答题 现有一可导热体积固定的密闭容器A,和一可导热容积可变的容器B.关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同.(已知:2NO2?N2O4;△H<0)
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA______VB.(填“>”、“<”、“=”);若打开活塞K2,气球B将______(填:变大、变小、不变).
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率αA将______(填增大或减小、不变);若通入等量的Ne气,则达到平衡时,A中NO2的转化率将______,B中NO2的转化率将______(填:变大、变小、不变).
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,______中的颜色较深.
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为______.
参考答案:(1)容器A中压强降低,容器B体压强不变,压强越大,反应速率越快,故v(A)<v(B),A中压强小于B中的压强,打开旋塞K,气球B的压强减小,体积减小,
故答案为:<;变小;
(2)保持容器容积不变,通入一定量的NO2,等效为增大压强到达的平衡,增大压强平衡向正反应方向移动,NO2的转化率将增大,故答案为:增大;
保持压强不变,通入氖气使体系的容积增大一倍,反应混合物的浓度降低,相当于为降低压强,平衡向逆反应方向移动,达到平衡时NO2的转化率减小,故答案为:变小;
(3)该反应为放热反应,A套上一个绝热层,温度升高,平衡逆向移动,NO2的浓度增大,颜色变深,故答案为:A;
(4)设参加反应的二氧化氮为xmol,n(NO2)=mM=4.6g46g/mol=0.1mol
2NO2 ?N2O4
起始的量:0.1mol 0
反应的量:x x2
平衡的量:0.1-xx2
平衡时平均相对分子质量=4.60.1-x+x2=57.5,所以x=0.04mol,所以平衡时平衡时N2O4的物质的量为:x2=0.02mol,
故答案为:0.02mol.
本题解析:
本题难度:一般
2、选择题 T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如图(Ⅰ)所示.若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如图(Ⅱ)所示.下列叙述正确的是( )

A.2?min内A的化学反应速率为0.1?mol/(L?min)
B.在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达平衡时,其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大
D.在T℃时,若A的浓度减少了1?mol/L,则B的浓度会减少3?mol/L,C的浓度会增加2?mol/L
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列图示与对应的叙述相符的是( )

A.图1表示可逆反应“2X(g)?Y(g)△H<0”,温度T1<T2的情形
B.用0.1000?mol?L-1NaOH溶液分别滴定浓度相同的三种一元酸,由图2曲线可确定①的酸性最强
C.在其它条件不变时,2SO2(g)+O2(g)?2SO3(g)转化关系(如图3)中,纵坐标表示O2的转化率
D.图4表示碳酸钙与盐酸反应收集到气体最多的时间段是t3~t4
参考答案:A
本题解析:
本题难度:简单
4、选择题 已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法正确的是( )
A.b代表0℃下CH3COCH3的Y-t曲线
B.反应进行到20min末,CH3COCH3的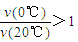
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的