��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� NaBH4����ˮ����ˮ��Ӧ��NaBH4��2H2O=NaBO2��4H2��������˵������ȷ���ǣ�NaBH4����HΪ��1�ۣ�?��?��
A��NaBH4�������������ǻ�ԭ��
B��NaBH4����������H2 O�ǻ�ԭ��
O�ǻ�ԭ��
C����Ԫ�ر���������Ԫ�ر���ԭ
D����������Ԫ��һ����ԭ��Ԫ������֮��Ϊ1��1
2��ѡ���� ���й������ڡ����Ĺ̶������ǣ�?��
A����������ѹ������ת��ΪҺ̬��
B��N2��O2���ŵ�����NO
C��NH3����������NO��H2O
D��NH3��H2SO4������������(NH4)2SO4
3��ѡ���� ��3�����NO2���壬����ͨ������3���ֱ�װ�Т�NaHCO3������Һ����ŨH2SO4����Na2O2��װ�ú�����ˮ���Ѳ��������ռ�������ƿ�У�����ƿ������Ӧ�ǣ�ͬ��ͬѹ�²ⶨ����?��
A��1���NO
B��2���NO2��0.5���O2
C��2���O2
D��0.25���O2
4��ѡ���� ����I����Cl����ϡ��Һ�е���AgNO3��Һ�����������������AgNO3��Һ����Ĺ�ϵ����ͼ��ʾ����ԭ��Һ��c(I-)/c (Cl-)�ı�ֵΪ?��?��
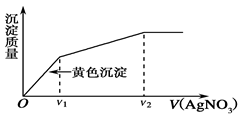


A��(V2��V1)/V1
B��V1/V2

C��V1/(V2��V1)
D��V2/V1
5�������� �����ǻ�ѧ��ҵ��Ӧ�÷dz��㷺�����ʡ���������������������Ҫ��;��
�������Ƽ���ķ���Ϊ�����й�������ҵ��������Ҫ���ס��Ƽ�ĵ�һ����Ӧ���Ͱ�����ˮ��ͨ�������̼���÷�Ӧ�ɱ�ʾΪ��NaCl + CO2 + NH3 + H2O �� NaHCO3��+ NH4Cl
����45��ʱ��ȡ117gʳ�����Ƴɱ�����Һ��������ͨ��������������������ͨ�������̼��ʹ��Ӧ������ȫ���Լ��㲢�ش��������⣨������ȡ��λ��Ч���֣����й����ʵ��ܽ�������������λ��g/100gˮ����
?
| NaCl
| NaHCO3
| NH4Cl
|
10��
| 35.8
| 8.15
| 33.0
|
45��
| 37.0
| 14.0
| 50.0
|
?
��1��117gʳ�������Ͽ�����ȡ����?g��
��2��45�淴Ӧ��Ϻ��о�����������Һ��ʣ��ˮ?g���������������?g��
��3�����˳�ȥ�����ľ�����ٽ�����10�棬���о������������������������������?��
��ҵ������Ҳ�ǰ�����Ҫ��;֮һ����Ӧ���£�
4NH3+5O2��4NO+6H2O? 2NO+O2��2NO2? 3NO2+H2O��2HNO3+NO
��a mol��NH3��b mol��O2��Ϻ���һ�ܱ���������Pt������������700�棬��ַ�Ӧ����ȴ�����¡�
 ��4��������b�Ma��ȡֵ��Χ����֮��Ӧ����Һ�����ʼ������ʵ���������������±��У�
��4��������b�Ma��ȡֵ��Χ����֮��Ӧ����Һ�����ʼ������ʵ���������������±��У�
b�Ma��ȡֵ��Χ
| ����
| �������ʵ���
|
?
| ?
| ?
|
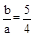
| ����
| ����
|
?
| ?
| ?
|
?
| ?
| ?
|
?