��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� 2�֣�25�棬��֪pH = 2�ĸߵ�����Һ��pH = 12��NaOH��Һ�������ϣ����û��Һ�����ԣ�pH = 2�ĸ�������Һ��pH = 12��NaOH��Һ�������ϣ����û��Һ�����ԡ��������Եĸߵ��ᱵ[Ba5(IO6)2]��ϡ�����ϣ�������Ӧ�����ӷ���ʽΪ��____________��
�ο��𰸣�5Ba2+ +2IO65-+10H+ +5SO42-=5BaSO4+2H5IO6
���������pH = 2�ĸߵ�����Һ��pH = 12��NaOH��Һ�������ϣ����û��Һ�����ԣ�˵���ߵ��������ᡣpH = 2�ĸ�������Һ��pH = 12��NaOH��Һ�������ϣ����û��Һ�����ԣ�˵����������ǿ�ᣬ�������ӷ���ʽΪ5Ba2+ +2IO65-+10H+ +5SO42-=5BaSO4+2H5IO6��
�����Ѷȣ�һ��
2��ѡ���� ��pHΪ5��������Һϡ��500����ϡ�ͺ���Һ��c (SO42������c (H+)ԼΪ
A��1��1
B��1��2
C��1��10
D��10��1
�ο��𰸣�C
���������������ϡ��ʱ��Ҫ����ˮ�ĵ���ƽ�⣬������ϡ��ʱ��Һ�е�������Ũ�Ƚӽ�10��7mol/L��pHΪ5��������Һ��Ũ����5��10��6mol/L������ϡ��500����c (SO42������1��10��8mol/L������ϡ�ͺ���Һ��c (SO42������c (H+)ԼΪ1�U10����ѡC��
�����Ѷȣ�һ��
3��ѡ���� 25��ʱ���Ͻ�ˮ����0.1mol/L�İ�ˮ�У�����ͼ��仯��������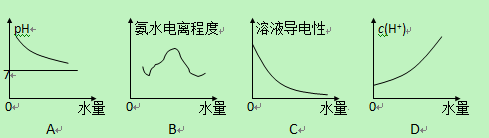
�ο��𰸣�AC
���������
ѡAC��
ϡ��ʱ����������Ũ���½���pH�½���������7��A�ԣ������ʼ������B��������Ũ���½������������½���C�ԣ�����������Ũ���½���������Ũ���������������䣬D��
�����Ѷȣ�һ��
4��ѡ���� �к͵ζ���ʼ��Ӧע�ӣ��ٵζ�����Һ��ı仯 ����ƿ����Һ��ɫ�ı仯 �۵ζ�����Һ����������
A���ٺ͢�
B���ں͢�
C���ٺ͢�
D��ֻ�Т�
�ο��𰸣�B
����������к͵ζ���ʼ�ͽ���ʱ������ʵ��ǰ��ʵ��������Һ��仯������ҩƷ�������������к͵ζ���ʼ��Ҳ���ǵζ��Ĺ����У�Ӧ��ע�������ƿ����Һ��ɫ�ı仯�Լ��ζ�����Һ���������ʣ��Ա���õĿ����к͵ζ��Ľ��̡�
�����������漰���к͵ζ�ʵ�飬��Ҫ���Ƶγ�Һ������ʣ��쵽�ζ��յ��ʱ����ƿ�еĿ�ʼ����ɫ�仯ʱ��Ҫ�������٣����ǹؼ���
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
[? ]
A��HCl��NaOH��Ӧ���к��ȡ�H=-57.3 kJ/mol����H2SO4��Ca(OH)2��Ӧ���к��ȡ�H=2��(-57.3) kJ/mol
B��CO(g)��ȼ������283.0 kJ/mol����2CO2(g)=2CO(g)+O2(g)��Ӧ�ġ�H=+2��283.0 kJ/mol
C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D��1mol����ȼ��������̬ˮ�Ͷ�����̼���ų��������Ǽ����ȼ����
�ο��𰸣�B
���������
�����Ѷȣ���