微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验需要0.80 mol・L-1 NaOH溶液 475mL和0.40 mol・L-1硫酸溶液500mL。根据这两种溶液的配制情况回答 下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是_______ (填仪器名称)。?
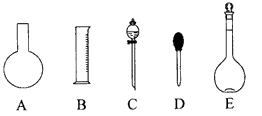
(2)下列操作中,容量瓶所不具备的功能有 ___________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为____g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度____0.8 mol・L-1(填“大于”“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度____0.8 mol・L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g・cm-3的浓硫酸的体积为_________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、 20 mL、50 mL量筒,应选用_________mL量筒最好。
参考答案:(1)A、C ;烧杯、玻璃棒
(2)C、E、F
(3)16.0? ;大于 ;等于
(4)10.9 ;15
本题解析:
本题难度:一般
2、实验题 配制一定物质的量浓度的溶液是实验室进行科学研究的重要环节。
(1)若配制大约1 mol・L-1 的溶液100 mL,所给仪器只有托盘天平、量筒、带刻度的烧杯、玻璃棒,下列可选用的试剂是________(填字母序号)。
A.氢氧化钠固体 B.浓硫酸(98%) C.浓盐酸(37%) D.浓硝酸(63%)
(2)下图所示是某学生在配制0.100 mol・L-1 的碳酸钠溶液100 mL时,将第一次洗涤液转移到容量瓶内的操作。
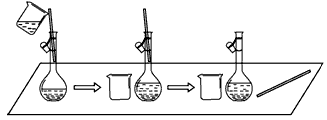
该步操作对所得溶液浓度的影响是__________(填“偏高”、“偏低”或“无影响”),原因是_____________________、___________、_____________。
(3)若配制(2)中溶液时,该生使用托盘天平称取碳酸钠,则与计算量一致吗?为什么?
____________________________________。
参考答案:(1)ABCD
(2)偏低;玻璃棒紧靠容量瓶口,造成洗涤液外溢;玻璃棒从容量瓶移出时,残留在玻璃棒上的洗涤液可能滴在瓶外;玻璃棒移出后直接放在桌面上,造成残留洗涤液损失
(3)不一致,因为碳酸钠的计算量为1.06 g,而托盘天平只能精确到0.1 g,即称取碳酸钠1.1 g
本题解析:
本题难度:一般
3、简答题 实验室用Na2SO4?10H2O配制0.1mol/L的Na2SO4溶液500ml.有以下仪器:
①药匙?②100ml量筒?③1000ml容量瓶?④锥形瓶?⑤玻璃棒?⑥烧杯
(1)配制时,必须选用的仪器为:______(填代号),还缺少的玻璃仪器为______
(2)经计算,本实验需称量硫酸钠晶体(Na2SO4?10H2O)为______g.
(3)用Na2SO4?10H2O配制标准溶液的正确顺序是______.
A.冷却?B.称量?C.洗涤?D.定容?E.溶解?F.摇匀?G.移液
(4)将所配制的Na2SO4溶液进行测定,发现浓度大于0.1mol/L.请你分析配制过程中可能引起该误差的原因是(填字母代号)______
①容量瓶不干燥,含有少量蒸馏水?②定容时俯视刻度线?③定容时仰视刻度线?④未冷却至室温就转移到容量瓶中?⑤没有洗涤烧杯和玻璃棒.
参考答案:(1)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒加水),用玻璃棒搅拌,加速溶解,恢复室温后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以需要的仪器有托盘天平、烧杯、玻璃棒、500ml的容量瓶、胶头滴管、药匙、量筒(可用可不用),
故必须选用的仪器为:①⑤⑥,还缺少的玻璃仪器为:500ml的容量瓶、胶头滴管,
故答案为:①⑤⑥,500ml的容量瓶、胶头滴管;
(2)硫酸钠的物质的量为0.5L×0.1mol?L-1=0.05mol,硫酸钠的物质的量等于硫酸钠晶体的物质的量,故需要硫酸钠晶体的质量为0.05mol×322g/mol=16.1g,
故答案为:16.1;
(3)由(1)溶液配制操作可知,正确顺序是BEAGCGDF,
故答案为:BEAGCGDF;
(4)①最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响,故不符合;
②定容时,俯视容量瓶刻度线,液面在刻度线以下,使溶液的体积偏小,所配溶液浓度偏高,故符合;
③定容时仰视刻度线,液面在刻度线以上,溶液体积偏大,所配溶液浓度偏低,故不符合;
④未冷却至室温就转移到容量瓶中定容,溶液冷却后,使溶液的体积偏小,所配溶液浓度偏高,故符合;
⑤没有洗涤烧杯和玻璃棒,少量硫酸钠沾在烧杯壁与玻璃棒上(洗涤液中含有少量硫酸钠),移入容量瓶中硫酸钠的实际物质的量减小,溶液浓度偏低,故不符合;
故选②④.
本题解析:
本题难度:一般
4、选择题 已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl.在标准状况下,向100mLFeCl3溶液中通入a?L的H2S气体恰好反应后,再加入足量的铁粉充分反应.所得溶液经测定金属阳离子的浓度为3mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为
A.1.5mol/L
B.2?mol/L
C.1?mol/L
D.无法确定
参考答案:B
本题解析:分析:该反应过程为:氯化铁和硫化氢反应生成氯化亚铁和盐酸,盐酸再和铁反应生成氯化亚铁,所以反应实质是氯化铁和铁反应生成氯化亚铁,根据氯原子守恒计算氯化铁的物质的量浓度.
解答:该反应过程为:氯化铁和硫化氢反应生成氯化亚铁和盐酸,盐酸再和铁反应生成氯化亚铁,所以反应实质是氯化铁和铁反应生成氯化亚铁,根据氯原子守恒计算氯化铁的物质的量浓度,
2FeCl3+Fe=3FeCl2,根据方程式知,c(FeCl3)=c(FeCl2)× =3mol/L×
=3mol/L× =2mol/L,
=2mol/L,
故选B.
点评:本题考查了物质的量的有关计算,明确反应实质是解本题关键,然后利用原子守恒进行分析解答即可,难度不大.
本题难度:困难
5、实验题 实验室用固体烧碱配制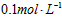 的NaOH溶液500mL,回答下列问题:
的NaOH溶液500mL,回答下列问题:
(1)计算需要固体NaOH的质量_____________g。
(2)有以下仪器和用品:① 烧杯 ② 药匙 ③ 250mL容量瓶 ④ 500mL容量瓶⑤ 玻璃棒 ⑥ 托盘天平配制时,必须使用的仪器或用品有_____________(填序号),还缺少的仪器是__________________。
(3)下列称量NaOH的操作中,正确的是_____________(填序号)
① 把NaOH直接放在托盘天平上称量 ② 把NaOH放在纸上称量 ③ 把NaOH放在小烧杯中上称量
(4)使用容量瓶前必须进行的一步操作是__________________。
(5)配制时,一般分为以下几个步骤: ① 称量 ② 计算 ③ 溶解 ④ 摇匀 ⑤ 转移 ⑥ 洗涤 ⑦ 定容 ⑧ 冷却 ⑨ 振荡。其正确的操作顺序为___________________。
(6)配制过程中,下列操作会引起结果偏高的是______________(填序号)
① 未洗涤烧杯、玻璃棒
② NaOH溶液未冷却至室温就转移到容量瓶
③ 容量瓶不干燥,含有少量蒸馏水
④ 称量NaOH的时间太长
⑤ 定容时俯视刻度
参考答案:(1)2.0g
(2)①②④⑤⑥;胶头滴管
(3)③
(4)检查容量瓶是否漏水
(5)②①③⑧⑤⑥⑨⑦④
(6)②⑤
本题解析:
本题难度:一般