��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��13�֣�����֬�ް�סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���۲쵽��֬����ȼ��������
��1��������ʵ���������õ����йع������Ƹ�ˮ��Ӧ�Ľ����ǣ���һ�����������ɣ��ڶ���?��Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽ��?��
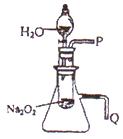
��2��ij�о���ѧϰС��������ͼ��ʾװ�ã����������ã�����ʵ�飬��֤���������ۡ�������֤��һ�����۵�ʵ������������ǣ�?��������֤�ڶ������۵�ʵ������������ǣ�?��
��3�����Թ��м�ˮ��������ȫ�ܽ��Ҳ������������ɺ�ȡ���Թܣ����Թ��е����̪��Һ��������Һ�ȱ�����ɫ��Ϊ̽����ԭ��С��ͬѧ�Ӳ����й������е�֪��Na2O2��ˮ��Ӧ������H2O2��H2O2����Ư���ԡ�
�����һ����ʵ�飬��֤Na2O2������ˮ��ַ�Ӧ�����Һ����H2O2���ڡ���ֻҪ��д��ʵ�����õ��Լ����۲쵽������
�Լ���?��
����?��
��4����С��ͬѧ����ö����ķ���̽��Na2O2��ˮ��Ӧ�����Һ���Ƿ���H2O2����ʵ�鷽��Ϊ����ȡ2.6g Na2O2���壬ʹ֮��������ˮ��Ӧ����������O2�������������ֵ�Ƚϣ����ɵó����ۣ�

�ٲ����������ʱ��������Թܺ���Ͳ�ڵ����嶼��ȴ������ʱ���У�Ӧѡ����ͼװ���еģ����Ե�������Ͳ����ռ�������?����A��B����������?��
�����ڱ�״���²�������������Ӧѡ�õ���Ͳ�Ĵ�С���Ϊ?��ѡ�100mL������200mL������500mL����1000mL����
�ο��𰸣�

�����������
�����Ѷȣ�һ��
2��ѡ���� ��11�֣�.AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ��������֮��������ͼת����ϵ��
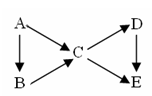
��1������ͼ��B��C��Ϊ�����D��E��Ϊ�Σ���A�����ǣ����ţ�__________��
��Na?��N2 ?��C?��S?
��2�����������ʵ���ɫ��Ӧ��Ϊ��ɫ������C��D��E��ˮ��Һ���Լ��ԣ��ҵ�Ũ��ʱ����C��D��E��B��������������B�к��еĻ�ѧ������Ϊ__________________��
Aת����C�����ӷ���ʽΪ��________________________________��
Dת����E�����ӷ���ʽΪ_______________________________________��
��3����������B��C��D��Ϊ���壬��B������ʹʪ��ĺ�ɫʯ����ֽ����
���ڹ�ҵ������B����ʱΪ�˼ӿ췴Ӧ����Ӧѡ���������______________����������߷�Ӧ���ת���ʵ�������___________��
��C��D������β���е��к��ɷ֣���NaOH��Һ���տ�������Ⱦ����Ӧ�Ļ�ѧ����ʽΪ__________________________________��
�ο��𰸣�����11�֣���1���٢ۣ�2�֣�?
��2�����Ӽ����Ǽ��Թ��ۼ����ۼ�������2�֣�2Na��2H2O��2Na+��2OH-��H2������1�֣�
CO32-��CO2��H2O��2HCO3?��1�֣�
��3���ٸ��¡���ѹ����������2�֣�?��ѹ��1�֣�
��NO��NO2��2NaOH��2NaNO2��H2O��2�֣�
���������
��1���٢�
��������A��C��2Na��O2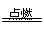 Na2O2,A��B��4Na��O2=2Na2O,B��C��2Na2O��O2
Na2O2,A��B��4Na��O2=2Na2O,B��C��2Na2O��O2 2Na2O2;
2Na2O2;
��A��C,������N2ֱ������NO2;
��A��C��C��O2 CO2��A��B��2C��O2="2CO" B��C��2CO��O2=2CO2;
CO2��A��B��2C��O2="2CO" B��C��2CO��O2=2CO2;
��A��C,������Sֱ������SO3;
��2�����Ӽ����Ǽ��Թ��ۼ����ۼ�������2�֣�2Na��2H2O��2Na+��2OH-��H2������1�֣�
CO32-��CO2��H2O��2HCO3?��1�֣�
������A��Na��B��ΪNa2O2��CΪNaOH��DΪNa2CO3��E ΪNaHCO3,B��ΪNa2O2��Na�� ��O22�D֮��Ϊ���Ӽ���O22�D��O�DO��Ϊ�Ǽ��Թ��ۼ����ۼ�����Aת����C�����ӷ���ʽΪ����2Na��2H2O��2Na+��2OH-��H2����Dת����E�����ӷ���ʽΪCO32-��CO2��H2O��2HCO3?
��3���ٸ��¡���ѹ����������2�֣�?��ѹ��1�֣�
��NO��NO2��2NaOH��2NaNO2��H2O��2�֣�
������A�DN2? B�DNH3? C�DNO? D�DNO2? E�DHNO3
���ڹ�ҵ������NH3����ʱΪ�˼ӿ췴Ӧ����Ӧѡ��������Ǹ��¡���ѹ����������������߷�Ӧ���ת���ʵ������Ǹ�ѹ;��C�DNO��D�DNO2������β���е��к��ɷ֣���NaOH��Һ���տ�������Ⱦ����Ӧ�Ļ�ѧ����ʽΪNO��NO2��2NaOH��2NaNO2��H2O��
�����Ѷȣ�һ��
3��ѡ���� ������������Һ�еμӼ���������Һ��һ���ܵõ���ɫ��������
A? Al2(SO4)3��Һ? B? CaCl2 ��Һ? C FeCl2��Һ? D? MgSO4��Һ
�ο��𰸣�D
���������A���ܣ����������������Ʒ�Ӧ��������������������������������Ҫ�ܽ��ڹ�����ǿ����Һ�С�
B���ܣ������������������Ӳ���Ӧ��
C���ܣ��������������������ӷ�Ӧ��������������������Ѹ�ٱ����������������������Ǻ��ɫ������
D���ԣ�þ���������������ӷ�Ӧ���ɰ�ɫ����������þ�������ڼ
�����Ѷȣ�һ��
4��ѡ���� ���������Ż�ʱ�����������������ʻ����ĵ���
A��ˮ
B��ɳ��
C��ú��
D����ĭ�����(��Ҫ�������CO2��ˮ�Ȼ��ǵ���ĭ״����)
�ο��𰸣�B
�����������
�����Ѷȣ���
5������� ��12�֣�̼���ƺ�̼�������������г��������ʡ���ش��������⡣
������1��̼�����ƵĻ�ѧʽ��___________���׳�___________����ˮ��Һ��___________�ԣ���ᡱ��������С�����
������2��̼�����ƿ�����θ�ᣨ0.2%��0.4%�����ᣩ���࣬��Ӧ�����ӷ���ʽΪ___________
����___________�������ʵ�����̼���ƺ�̼���������������ᷴӦʱ����CO2������ǰ��___________���ߣ����������������������
������3����ȥ̼���ƹ�����̼�����Ƶķ�Ӧ�Ļ�ѧ����ʽΪ______________________��
�ο��𰸣���1��NaHCO3��С�մ�
������2��HCO3-+H+="=" CO2��+ H2O =
������3��2NaHCO3 Na2CO3 + H2O + CO2��
Na2CO3 + H2O + CO2��
�����������
�����Ѷȣ���