微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验是研究化学的基础,图模中所示的实验方法、装置或操作完全正确的是
[? ]
A.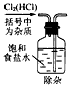
B.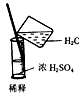
C.
D.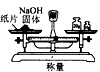
2、选择题 下列化学药品与其危险化学品图形标志不一致的一组是
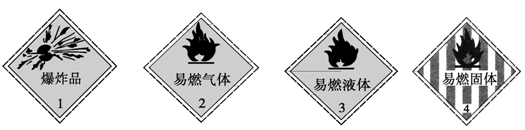
A.烧碱―1
B.甲烷―2
C.酒精―3
D.白磷―4
3、选择题 (9分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一 。其工艺流程如下:
。其工艺流程如下:
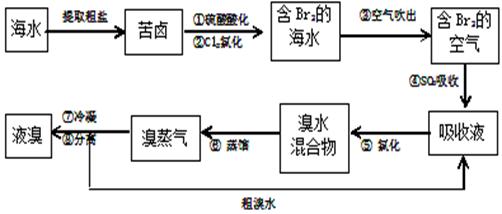
(1)溴在周期表中位于?周期,?族。
(2)步骤④的离子方程式:?。
(3)已知溴的沸点是58.5℃,步骤⑥的蒸馏过程中,溴出口温度为何要控制在80―90℃。温 度过高或过低都不利于生产 ,请解释原因:?。
度过高或过低都不利于生产 ,请解释原因:?。
(4)步骤⑧中溴蒸气冷凝后 得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是?,分离时液溴从分离器的?(填“上口”或“下口”)排出。
得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是?,分离时液溴从分离器的?(填“上口”或“下口”)排出。
(5)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”: ?。
?。
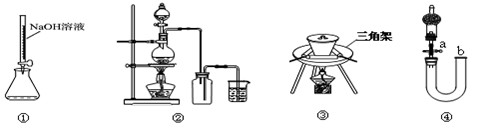
4、选择题 下图装置或操作正确的是
 ?
?
A.用装置①量取15.00ml的NaOH溶液
B.用装置②制备Cl2
C.用装置③高温煅烧CaCO3固体
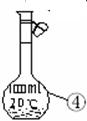
D.关闭活塞a,从b处加水,以检查装置④的气密性
5、实验题 (1)写出下图中序号①~④仪器的名称:
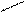
 ?
? ?
? ? I? II? III
? I? II? III
①?;②??;?③??;④ ?;
(2)仪器①~④中,使用时必须检查是否漏水的有??。(填仪器序号)
(3)分离碘水中的碘应先选择装置?(填装置序号)进行??和??操作,再用装置?(填装置序号)进行??操作。
(4)现欲用98%的浓硫酸(密度为1.84g・cm-3)配制成浓度为0.5mol・L-1的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需 __________、 __________、 __________。
②所取浓硫酸的体积为____________mL。
③下列操作引起所配溶液浓度偏高的是??
A 取浓硫酸时俯视
B 将浓硫酸倒出后,洗涤装置,并将洗涤液倒入烧杯中
?C 在烧杯中稀释浓硫酸后,立即转移
D 定容时俯视
E ?颠倒摇匀后发现液面低于刻度线,但未加水至刻度线