微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)(1)现用氯化铜晶体(CuCl2.2H2O,含少量FeCl2杂质)制取纯净的CuCl2.H2O先将其制成水溶液,后按如图步骤进行提纯:
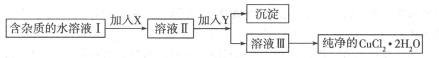
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表[来源:91exam.org]
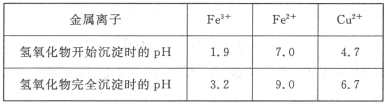
请回答下列问题:
①请从下列物质中选出第一步中需加入的X
a.NaClO b.H2O2
c.KMnO4 d.HNO3
②如何检验溶液Ⅱ中除Cu2+外的金属阳离子:________________________________。
③由溶液Ⅲ得到CuCl2.2H2O晶体的操作是___________________________________.
(2)某化学兴趣小组取一定量的双氧水,欲准确测定其中H2O2的含量:
取双氧水25. 00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准溶液滴定,其反应的离子方程式为: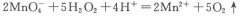
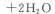
(1)滴定时,将高锰酸钾标准溶液注入________(填“酸式”或“碱式”)滴定管中,滴定到达终点的现象是________________________________________________
(2)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____(填“偏高”或“偏低”或“不变”)。
参考答案:(1)①b,②取少量溶液与试管中,加入少量硫氰化钾溶液,溶液显红色,证明含有铁离子(或用氢氧化钠法)③蒸发浓缩,冷却结晶。(2)酸式,溶液由无色变紫红色,且30秒内不褪色。(3)偏高。
本题解析:(1)①因为要分离铜离子和亚铁离子,根据氢氧化物开始沉淀时的pH时分析,当亚铁离子开始沉淀时,铜离子已经沉淀完全,铁离子开始沉淀,到沉淀完全,铜离子没有开始沉淀,所以需要将铁元素转化为铁离子进行分离,将亚铁离子变成铁离子需要加入一种氧化剂,但不能引入新的元素或杂质,所以选择b过氧化氢。②溶液Ⅱ中的除了铜离子以外的金属阳离子是铁离子,利用铁离子和硫氰化钾反应生成红色进行检验,所以操作为取少量溶液与试管中,加入少量硫氰化钾溶液,溶液显红色,证明含有铁离子(或利用铁离子和氢氧化钠生成红褐色沉淀的方法)。③溶液Ⅲ中含有的氯化铜,要得到带结晶水的晶体,需要将溶液蒸发浓缩,然后冷却结晶。(2)因为高锰酸钾一般都是酸性的溶液,且高锰酸钾有强氧化性,能氧化腐蚀橡胶管,所以选择酸式滴定管,滴定的终点为溶液由无色变紫红色,且30秒内不褪色。(3)若滴定前有气泡,滴定后消失,说明读数偏大,则测定的结果偏高。
考点:物质的分离和提纯,中和滴定实验的操作和误差分析。
本题难度:困难
2、填空题 写出下列物质在水溶液中的电离方程式。
(1) H2SO4:___________。
(2) NaHSO4:___________。
(3) NH4HCO3:___________。
(4) KOH:________。
(5) Ba(OH)2:________。
参考答案:(1)H2SO4=2H++SO42-
(2)NaHSO4=Na++H++SO42-
(3)NH4HCO3=NH4++HCO3-
(4)KOH=K++OH-
(5)Ba(OH)2=Ba2++2OH-
本题解析:
本题难度:一般
3、选择题 某温度下,向一定体积的0.1mol/L醋酸溶液中逐滴加入0.1mol/LNaOH溶液,溶液中pOH【注:pOH=-lgc(OH-)】与pH的变化关系如图所示,则下列说法中正确的是

A.M点所示溶液中c(Na+)