��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪�����������ת��

�Իش𣺣�1��д��B�Ļ�ѧʽ______��D�Ļ�ѧʽ______��
��2��д����Eת���F�Ļ�ѧ����ʽ______��
��3��д����KSCN����G��Һ�����ӷ���ʽ______��
�ο��𰸣���ɫ����EΪFe��OH��2�����ɫ����FΪFe��OH��3��D��Һ���������ữ�����������ɰ�ɫ����HΪAgCl�����ɵ���Һ�к��м����ӣ�֤��D��ҺΪKCl������ת����ϵ�õ���CΪKOH��BΪFeCl2��F�ܽ������ᣬ˵���������ܽ����ɵ�GΪFeCl3���ж�AΪFe��
��1�������ƶ�B�Ļ�ѧʽΪ��FeCl2��D�Ļ�ѧʽΪ��KCl���ʴ�Ϊ��FeCl2��KCl��
��2��E��Fe��OH��2��ת���F��Fe��OH��3���ķ�Ӧ������������������Ϊ������������Ӧ�Ļ�ѧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3
��3��д����KSCN����G��FeCl3����Һ�����õ������������Ӻ�������������γ�Ѫ��ɫ��Һ����Ӧ�����ӷ���ʽΪ��Fe3++3SCN-=Fe��SCN��3��
�ʴ�Ϊ��Fe3++3SCN-=Fe��SCN��3��
���������
�����Ѷȣ�һ��
2������� A��B��CΪ3�ֵ���(����AΪ���壬B��CΪ����)��D����ҺΪ�ػ�ɫ��������������Һ����ֺ��ɫ������B��C��Ӧ�IJ���������ˮ�õ���ɫ��ҺE������֮���ת����ϵ��ͼ��

��д���пհף����ʣ�д��ѧʽ��A��______ B��______
C��______D ��??E ��??F��?
�ο��𰸣�
�����������
�����Ѷȣ�һ��
3������� ��֪A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE������֮��ת����ϵ��ͼ��ʾ��
��1��д��D��A��Ӧ�����ӷ���ʽ��
D+A��______��
��D��Һ�еμ����軯�أ���Һ��Ϊ��ɫ��������ӷ���ʽ��______��
��2��д����F�м���NaOH���ڿ����з����������ķ�Ӧ�Ļ�ѧ����ʽ���漰�����仯����______��______��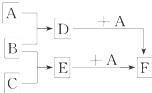
�ο��𰸣�A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��D���Ȼ�����A��B���ǵ��ʣ���A�ǹ��壬����A������B��������B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE����C��������E���Ȼ��⣬���������Ӧ�����Ȼ���������F���Ȼ�������
��1���Ȼ���������Ӧ�����Ȼ����������ӷ�Ӧ����ʽΪ��2Fe3++Fe�T3Fe2+�������Ӻ����軯����Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ�����ӷ�Ӧ����ʽΪ��Fe3++3SCN-�TFe��SCN��3��
�ʴ�Ϊ��2Fe3++Fe�T3Fe2+��Fe3++3SCN-�TFe��SCN��3��
��2���Ȼ��������������Ʒ�Ӧ���ɰ�ɫ�����������������������������ȶ����ױ������������ɺ��ɫ������������Ӧ����ʽΪ��FeCl2+2NaOH�TFe��OH��2��+2NaCl��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ��FeCl2+2NaOH�TFe��OH��2��+2NaCl��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���������
�����Ѷȣ���
4������� ͼ��A��G��Ϊ��ѧ��ѧ�г��������ʣ�����֮��������ת����ϵ������A��GΪ�ǽ������ʣ�AΪ��ɫ���塢GΪ��̬��D��F���Ǵ�����Ⱦ���Ҫ��Դ������β��������DΪ����ɫ����ش��������⣺
��1��AԪ����Ԫ�����ڱ���λ��______����______�壬C�Ļ�ѧʽ��______��
��2��д��D��E��Ӧת��ΪF��B�Ļ�ѧ����ʽ______��
��3���ڳ����£�B��ϡ��ҺҲ����Cu��Ӧ����F���˷�Ӧ�����ӷ���ʽ��______��
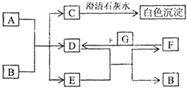
�ο��𰸣�D��F���Ǵ�����Ⱦ���Ҫ��Դ������β�����ƶ�Ϊ�����������DΪ����ɫ�ж�ΪNO2��FΪNO��GΪO2��C��ת����ϵ��C�ͳ���ʯ��ˮ��Ӧ����̼��Ƴ�����֤��CΪ����ΪCO2��D��NO2��+E=F��NO��+B���ƶ�EΪH2O��BΪHNO3��A��GΪ�ǽ������ʣ�AΪ��ɫ���塢GΪ��̬���ж�AΪC��֤��CΪ������̼��
��1��AԪ��Ϊ̼Ԫ�أ������ڱ���λ��Ϊ�ڶ����ڵڢ�A�壬CΪCO2���ʴ�Ϊ���ڶ�����A��CO2��
��2��DΪNO2��EH2O��Ӧת��ΪF��NO����B��HNO3���Ļ�ѧ����ʽΪ��3NO2+H2O=2HNO3+NO���ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��3�������£�B��HNO3����ϡ��ҺҲ����Cu��Ӧ����F��NO������Ӧ�����ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
���������
�����Ѷȣ�һ��
5������� ����A��E��F����ɫ��Ӧ�ʻ�ɫ������I�ķ�����4��ԭ����ɲ�������10�����ӣ�B��C��D��K�ڳ����¶������嵥�ʣ�G�ڳ���������ɫҺ�壬��Ӧ�١��ݶ������ڹ�ҵ�����ķ�Ӧ�����й�����֮������Ӧת����ϵ��ͼ��ʾ��

����д���пհף�
��1��д���������ʵĻ�ѧʽ��B��______��J��______��
��2��д�����з�Ӧ�ķ���ʽ���ٷ�Ӧ�ٵ����ӷ���ʽ��______���ڷ�Ӧ�ݵĻ�ѧ����ʽ��______��
��3����ͨ��״���£���1g?C������B������ȼ������H����ʱ�ų�92.3kJ��������2mol?H������ȫ�ֽ�����C�����B������Ȼ�ѧ����ʽΪ��______��
�ο��𰸣�I�ķ�����4��ԭ����ɲ�������10�����ӣ�ӦΪNH3��G�ڳ���������ɫҺ�壬ӦΪH2O����ת����ϵ��֪��Ӧ��ӦΪ�����Ĵ���������KΪO��JΪNO����CΪH2��DΪN2������A��E��F����ɫ��Ӧ�ʻ�ɫ��Ӧ��������Ԫ�أ�M�ڹ��������¿�����O2��ӦΪHClO����HΪHCl��BΪCl2��EΪNaClO��AΪNaOH��FΪNaCl��
��1�������Ϸ�����֪BΪCl2��JΪNO���ʴ�Ϊ��Cl2��NO��
��2���ٷ�Ӧ��Ϊ�������������Ƶķ�Ӧ����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
�ڷ�Ӧ��Ϊ�����Ĵ�������Ӧ����Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2����.��4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2����.��4NO+6H2O��
��3����1g?H2������Cl2������ȼ������H����ʱ�ų�92.3kJ��������1molH2ȼ�շų�184.6kJ����������2HCl��g��=H2��g��+Cl2��g������H=+184.6?kJ?mol-1��
�ʴ�Ϊ��2HCl��g��=H2��g��+Cl2��g������H=+184.6?kJ?mol-1��
���������
�����Ѷȣ�һ��