微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 已知甲、乙、丙、丁均为短周期元素组成的物质,它们之间的反应关系如下图所示
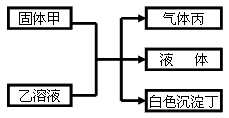
(1)若丙是元素A的气态氢化物,丙能与A的最高价氧化物的水化物反应生成盐B;乙是一种正盐,与B含有相同的阳离子;丁不溶于稀硝酸。则甲的化学式为______,乙溶液中各离子浓度由大到小的顺序为
__________________。
(2)若甲是短周期主族元素中原子半径最大的元素组成的单质,丁既可溶于盐酸又可溶于NaOH溶液。若甲和乙中的金属阳离子以3:1的物质的量之比在溶液中充分反应,则该反应的离子方程式为___________________________。
(3)若丙是一种四原子核分子,分子中四个原子在一条直线上;甲与乙溶液反应只生成气体丙、CaCO3和H2O,则丙的电子式为____________,乙的化学式为____________。
参考答案:
(1)Ba(OH)2;C(NH4+)>C(SO42-)>C(H+)>C(OH-)
(2)6Na + 2Al3+ + 6H2O = 6Na+ + 2Al(OH)3↓ + 3H2↑或2Na + 2H2O=2Na+ + 2OH- + H2↑、3OH-+ Al3+ =
Al(OH)3↓?
(3)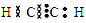 ;Ca(HCO3)2
;Ca(HCO3)2
本题解析:
本题难度:一般
2、填空题 (13分)根据下面图示,回答下列问题。(已知A是常见金属单质)

(1)?写出A、B、C、D、E的化学式
A:??B:??
C:??D:?
E:?
(2)按要求书写化学方程式
①E B ??
B ??
②放置生成D??
③E具有净水作用,反应原理是________________________________
④工业上炼制A的最主要反应方程式? _________________________________
参考答案:(1)A? Fe?,B FeCl2 ?,C KCl?,D Fe(OH)3?,E? FeCl3?。(各1分)
(2)①E B? 2 FeCl3 +Fe=3 FeCl2?
B? 2 FeCl3 +Fe=3 FeCl2?
②放置生成D? 4 Fe(OH)2? +O2 ?+2H2O ="4" Fe(OH)3?
③E具有净水作用,反应原理是FeCl3+3H2O=3HCl+Fe(OH)3
④工业上炼制A的主要反应方程式? Fe2O3+3CO=3CO2+2Fe(方程式各2分)
本题解析:略
本题难度:一般
3、填空题 (10分) A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y
的单质是生活中常见的金属,相关物质间的关系如下图所示。

(1)X的单质与A反应的化学方程式是______________________________________。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是____________________________。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是________________________________________
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)_______________________________。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是_________________________________。
参考答案:(1)Fe2O3+2Al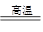 Al2O3+2Fe
Al2O3+2Fe
(2)2Al+2H2O+2OH-===2AlO+3H2↑
(3)①取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,证明原溶液中含有Fe3+
②Al3++3H2O? ?Al(OH)3+3H+
?Al(OH)3+3H+
③2FeSO4+2NaNO2+H2SO4===2Fe(OH)SO4+Na2SO4+2NO↑(3分)
本题解析:(1)元素X、Y的单质是生活中常见的金属,且X能置换出Y,则X是铝,Y是铁。则A是氧化铁,Y是氧化铝。所以X的单质与A反应的化学方程式是Fe2O3+2Al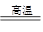 Al2O3+2Fe。
Al2O3+2Fe。
(2)铝能与氢氧化钠溶液反应生成氢气和偏铝酸钠,反应的方程式是2Al+2H2O+2OH-===2AlO+3H2↑。
(3)①若试剂1和试剂2均是稀硫酸,则D是氯化铁。检验铁离子的试剂是KSCN溶液,因此方法是取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,证明原溶液中含有Fe3+。
②铝离子在水溶液中水解生成氢氧化铝和氢离子,从而溶液显酸性,方程式是Al3++3H2O? ?Al(OH)3+3H+。
?Al(OH)3+3H+。
③根据反应物和生成物可知,反应的方程式是2FeSO4+2NaNO2+H2SO4===2Fe(OH)SO4+Na2SO4+2NO↑。
本题难度:一般
4、推断题 下图每一方框中的字母代表一种反应物或生成物:
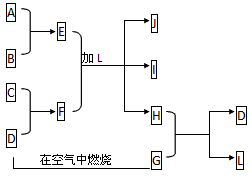
产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为:____________。
(2)F的化学式为:__________。
(3)写出J受热分解反应的化学方程式:______________________。
(4)H和G之间反应的化学方程式为:____________________。
参考答案:(1)H2O
(2)Na2S
(3)2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
(4)2H2S+SO2==3S+2H2O
本题解析:
本题难度:一般
5、填空题 (15分)钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减小环境污染。请填写下列空白:

(1)电解饱和食盐水时,该反应的离子方程式是____________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s);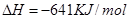
②

则 ____________
____________
反应:

 在Ar气氛中进行的理由是________
在Ar气氛中进行的理由是________
(3)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式______________________
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,该燃料电池发生反应时正极区溶液的PH_____(填“增大”、“减小”或“不变”)该电池中负极上的电极反应是__________.
(5)在上述产业链中合成96t甲醇理论上消耗H2_________t(不考虑生产过程中物质的任何损失)
参考答案:(1)(2分)2Cl-+2H2O  Cl2↑+H2↑+2OH-?
Cl2↑+H2↑+2OH-?
(2)-512 KJ/mol (2分)
Mg和Ti都有较强还原性,在高温下都易与空气中的O2反应(2分)
(3)2FeTiO3+6C+7Cl2 2FeCl3+2TiCl4+6CO(3分)
2FeCl3+2TiCl4+6CO(3分)
(4)增大(2分)? CH3OH-6e-+8OH-=CO32-+6H2O(2分)?(5)12?(2分)
本题解析::(1)电解食盐水生成NaOH、H2和Cl2,
利用盖斯定律2①-②即可计算出反应热为-512 KJ/mol。由于Mg和Ti都有较强还原性,在高温下都易与空气中的O2反应,所以反应要在Ar气氛中进行。
(3在碱性环境中正极: O2 + 4e- + 2H2O= 4OH- ,所以正极附近的碱性增强。负极甲醇发生氧化反应,CH3OH-6e-+8OH-=CO32-+6H2O
(5)CO(g)+2H2(g)←→ CH3OH(g)
4?32
X? 96t
x="12" t
点评:本题以学生不熟悉的金属钛(Ti)为题眼,结合化学工艺,考查的知识面广,但是设计的知识点简单。注重对基础知识点的考查。
本题难度:一般