微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (4分)将足量AgCl分别放入:①5ml水②10ml 0.2mol・L-1 MgCl2溶液③20ml 0.5mol・L-1 NaCl溶液,④40ml 0.1mol・L-1盐酸中溶解溶解至溶液饱和,各溶液中Ag+的浓度分别为a、b、c、d,它们由大到小的排列顺序是_____________________;0.2mol・L-1 NH4Cl溶液中离子浓度大小关系是_______________。
参考答案:a>d>b>c?c(Cl-)>c(NH4+)>c(H+) > c(OH-)
本题解析:AgCl在溶液中存在溶解平衡Ag(s)  ?Cl-(aq)+Ag+(aq),所以氯离子浓度越大,
?Cl-(aq)+Ag+(aq),所以氯离子浓度越大,
Ag+的浓度就越小。②③④中氯离子的浓度分别是0.4mol/L、0.5 mol/L、0.1 mol/L,所以顺序是a>d>b>c;NH4Cl溶液中由于NH4+的水解而显弱酸性,但水解程度很弱,所以大小顺序是
c(Cl-)>c(NH4+)>c(H+) > c(OH-)。
本题难度:一般
2、选择题 一定温度下,三种碳酸盐MCO3(M2+:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: p(M2+)=-lg c(M2+),p(CO32-)=-lg c(CO32-)。下列说法正确的是
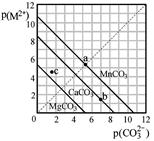
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.在100mL MgCO3、CaCO3、MnCO3饱和的混和溶液中加入足量浓K2CO3溶液,产生沉淀MnCO3质量最多
C.b点可表示CaCO3的饱和溶液,且Ca2+浓度与CO32-浓度相等
D.c点若表示MgCO3则为不饱和溶液,若表示CaCO3则有沉淀析出
参考答案:D
本题解析: A、根据图像分析坐标P值越大离子浓度越小,所以MnCO3的Ksp最小,错误;B、MgCO3溶解度最大,加入足量浓K2CO3溶液,产生沉淀质量最多,错误;C、曲线上的点表示饱和溶液,但b点Ca2+浓度大于CO32-浓度,错误;D、正确。
本题难度:一般
3、填空题 (13分)高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:

根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式 。
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10―38,除杂后溶液中c(Fe3+)约为 。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是 。
(5)“分离”操作的名称是 (填字母代号)。
A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2・12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是 ,离子浓度最小的离子是 。
参考答案:(13分) (1) 2Fe2++H2O2+4NH3・H2O=2Fe(OH)3↓+4NH4+
(2)4×10―20mol/L(3分)。(3)抑制(防止)Al3+水解。(2分)
(4)防止晶体失去结晶水,避免可溶性杂质结晶析出(2分,答对1点给1分)。
(5)C(1分)。(6)SO42―,OH―。(共2分,各1分)
本题解析:(1)H2O2可以把Fe2+氧化为Fe3+,然后加入氨水,就会形成Fe(OH)3沉淀而过滤除去,反应的离子方程式是2Fe2++H2O2+4NH3・H2O=2Fe(OH)3↓+4NH4+;(2)pH=8.0,则c(OH―)=10-6mol/L,在通常条件下Ksp〔Fe(OH)3〕=c(Fe3+)・c3(OH―)=4.0×10―38,所以c(Fe3+)= Ksp〔Fe(OH)3〕÷c3(OH―)= 4.0×10―38÷10-18=4×10―20mol/L;(3)硫酸铝是强酸弱碱盐,水解产生氢氧化铝胶体和硫酸,加入硫酸就可以抑制盐电离产生的Al3+的水解;(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干是因为蒸干容易使晶体失去结晶水,这样还避免可溶性杂质结晶析出;(5)把晶体从混合物中“分离”操作的名称是过滤;(6)铵明矾晶体的化学式为NH4Al(SO4)2・12H2O,在0.1mol/L在铵明矾的水溶液中,根据物料守恒可知离子浓度最大的离子是SO42―,由于该盐是强酸弱碱盐,NH4+、Al3+水解消耗水电离产生的OH-,使溶液显酸性,所以离子浓度最小的离子是OH―。
考点:考查物质制取的知识,包括反应条件的选择、离子方程式的书写、溶度积常数的应用、盐的水解、离子浓度的大小比较的知识。
本题难度:困难
4、选择题 已知25 ℃时,AgCl 的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液为AgCl的饱和溶液
B.AgNO3溶液与NaCl溶液混合后的溶液中,;一定有c(Ag+)=c(Cl-)
C.向饱和AgCl水溶液中加入盐酸,Ksp值变大
D.将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度小于AgI
参考答案:A
本题解析:溶度积常数是在溶解达到平衡状态时的定值,所以A正确;B不正确,因为溶液不一定是饱和溶液,二者的浓度不一定相等;溶度积常数只与温度有关系,所以C中溶度积是不变的,C不正确;D不正确,沉淀转化的方向一般是向溶解度更小的方向进行,所以AgCl溶解度大于AgI的,D不正确,答案选A。
点评:溶解平衡也是一种动态平衡,适用于勒夏特例原理。另外溶度积常数是在沉淀达到溶解平衡时,溶液中离子浓度的幂之积,该平衡常数与化学平衡常数一样,也只和温度有关系,据此可以进行有关的判断。
本题难度:一般
5、选择题 下列说法正确的是
[? ]
A.已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+)=0.1?mol・L-1,则此时溶液中存在:c(Na+)=c(CH3COO-)?>?c(CH3COOH)?>?c(H+)?=c(OH-)
B.0.01?mol・L-1的Na2HPO4溶液中存在如下的平衡:HPO42-+H2O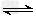 ?H2PO4-+OH-?HPO42-
?H2PO4-+OH-?HPO42-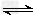 ?H++PO43- 且溶液pH>7;加水稀释后溶液中HPO43-、PO43-、H+的浓度均减小
?H++PO43- 且溶液pH>7;加水稀释后溶液中HPO43-、PO43-、H+的浓度均减小
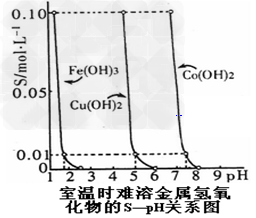
C.上图中,Y轴S表示相应金属氢氧化物在饱和溶液中阳离子的浓度,由图中数据可计算出室温下Ksp[Cu(OH)2]=1.0×10-12?
D.由上图可知,若Fe(NO3)3?溶液中含有少量的Co2+杂质,可通过加入Fe(OH)3的方法来除去
参考答案:A
本题解析:
本题难度:一般